
慢性肾脏病(CKD)是全球范围内疾病负担较重的疾病之一,2019年位列全球第11大死因,预计到2050年将上升至第10位。终末期肾病患者需要依赖透析或肾移植等肾替代疗法(RRT),但由于治疗可及性不足,全球仍有大量患者无法获得充分救治。细胞外囊泡(EVs)作为细胞间通讯的天然介质,被视为一种有潜力的无细胞治疗工具。然而,EVs在体内半衰期短(约2-4分钟)、清除快、靶向效率低,限制了其临床转化。
近期,葡萄牙米尼奥大学Nuno M. Neves团队在Biomaterials期刊发表题为“3D bioprinting meets nanotherapeutics: a vehicle for sustained extracellular vesicle delivery”的研究,开发了一种完全由脱细胞肾脏细胞外基质(DKECM)构成的生物墨水,实现了对肾祖细胞(RPCs)来源EVs的3D生物打印与持续释放,并验证了其在肾脏修复中的潜力。
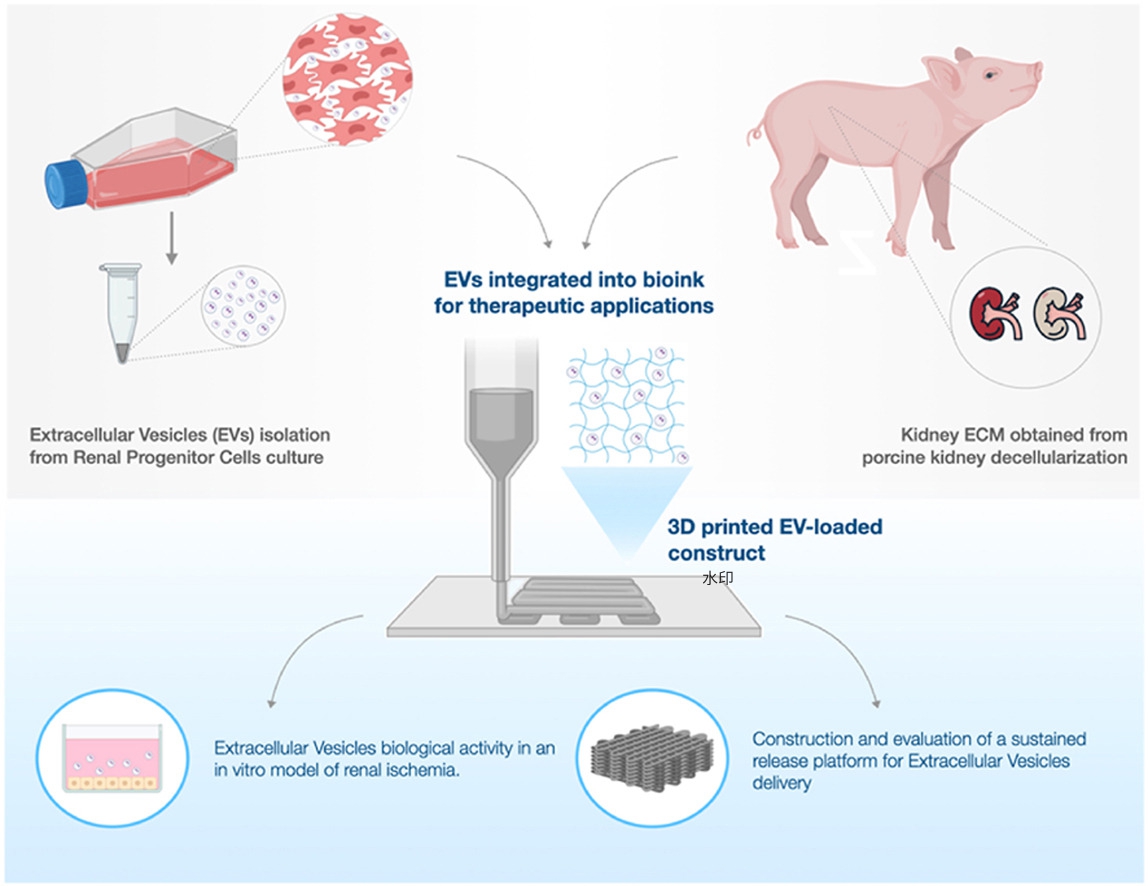
图形摘要
(点击图片查看大图)
研究内容
为获得具有肾脏特异性的治疗性EVs,研究团队首先从人肾祖细胞(RPCs)中分离并纯化了EVs。采用超滤联合尺寸排阻色谱(SEC)的方法,EVs纯度显著提高,蛋白污染减少97%,颗粒浓度提升超过300%。纳米颗粒追踪分析(NTA)显示EVs平均粒径为157 nm,冷冻电镜(Cryo-EM)观察到典型的囊泡形态,且EVs特异性标志物CD9、CD63、CD81及Syntenin-1均呈阳性,而线粒体蛋白Cytochrome-C为阴性,排除了细胞污染。上述结果表明,该方法可获得较高纯度、结构完整的RPCs来源EVs。(图1)
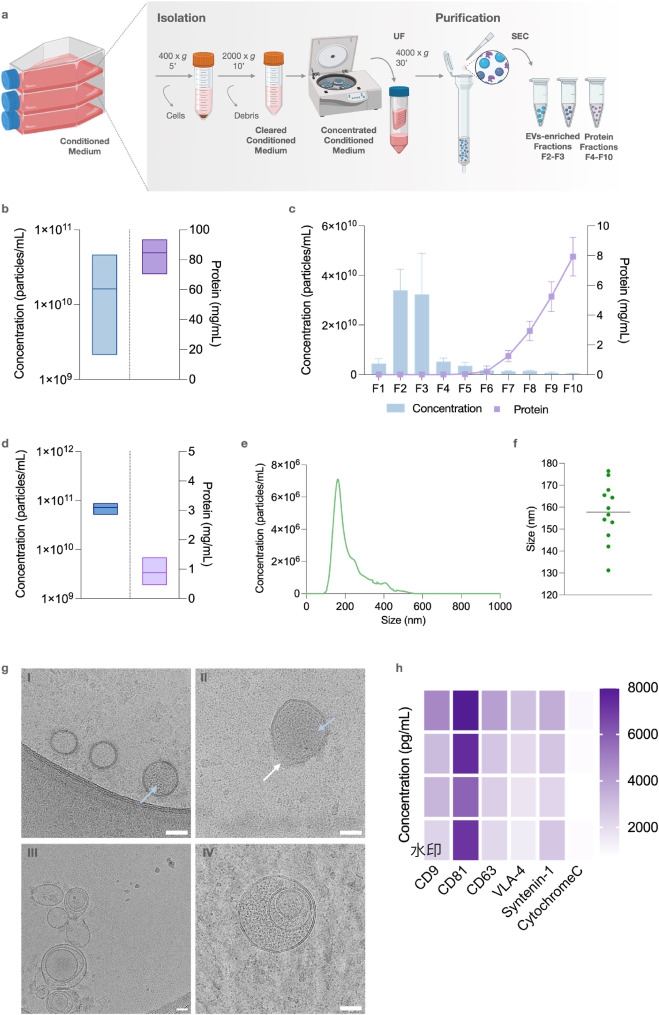
图1. 从人肾祖细胞中分离与表征细胞外囊泡
(点击图片查看大图)
随后,研究团队在体外缺氧模型中验证了RPCs来源EVs对肾小管上皮细胞(HK-2)的功能调控作用。结果显示,EVs处理可降低缺氧诱导的过度增殖(Ki67阳性细胞减少),下调损伤相关转录因子SOX9表达约40%,并降低活性氧(ROS)水平,提示EVs具有抗氧化应激和调节损伤-修复平衡的作用。而EVs对HK-2细胞的迁移能力无显著影响。(图2)
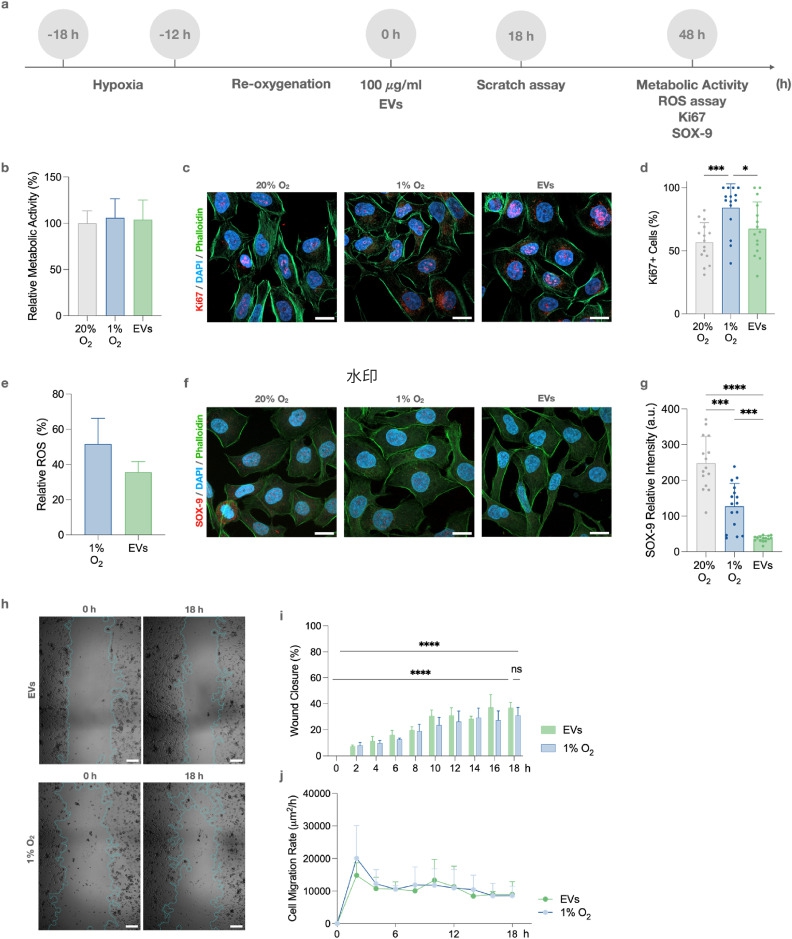
图2. 肾祖细胞来源EVs调控缺氧状态下肾小管上皮细胞的功能响应
(点击图片查看大图)
为实现EVs的局部、持续递送,研究团队制备了一种仅由脱细胞猪肾细胞外基质(DKECM)构成的生物墨水。组织学与DNA定量分析显示,脱细胞后细胞核被清除,残留DNA为22 ng/mg组织,低于免疫安全性阈值(50 ng/mg)。同时,不溶性胶原和糖胺聚糖(GAGs)等基质成分得以保留。流变学测试表明,该生物墨水具有剪切变稀、快速自愈合和温敏交联(37°C成胶)等特性,适用于后续3D生物打印。(图3)
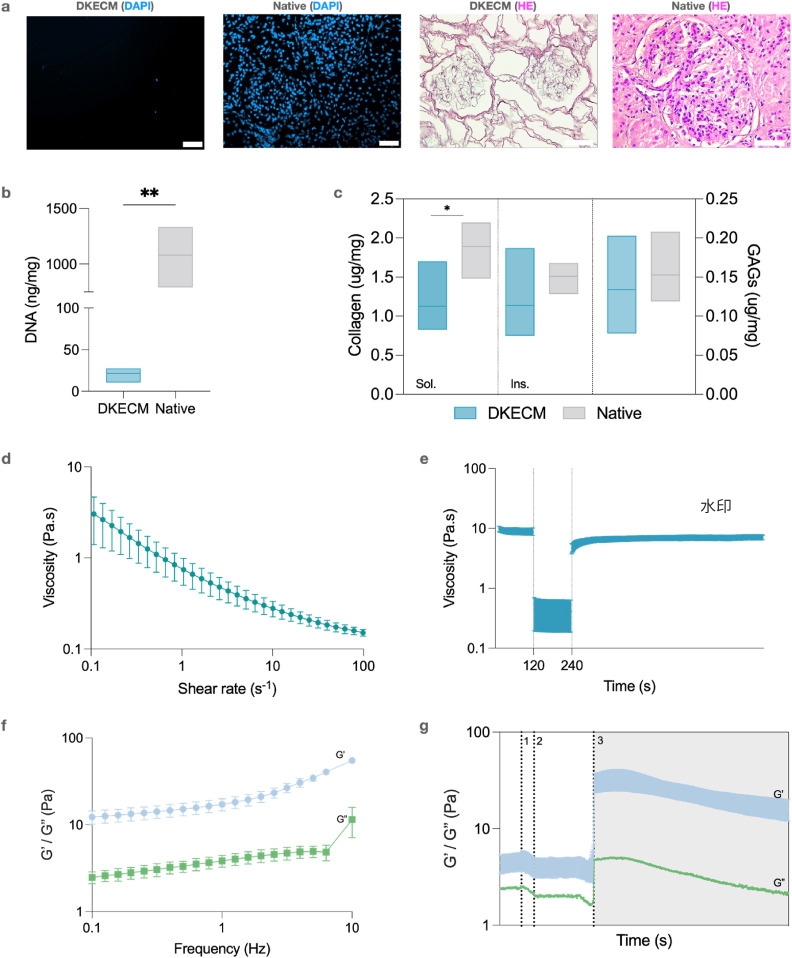
图3. 脱细胞肾脏细胞外基质生物墨水的制备与表征
(点击图片查看大图)
在可打印性评估中,DKECM生物墨水在琼脂糖微粒支撑浴中打印出4层和8层结构,纤维均匀、孔隙连通,打印参数(压力、速度、填充密度)可调控。纤维宽度和横截面积随打印速度增加而减小,表现出可控的挤出行为。该结果说明DKECM生物墨水具备构建多层结构的能力。(图4)
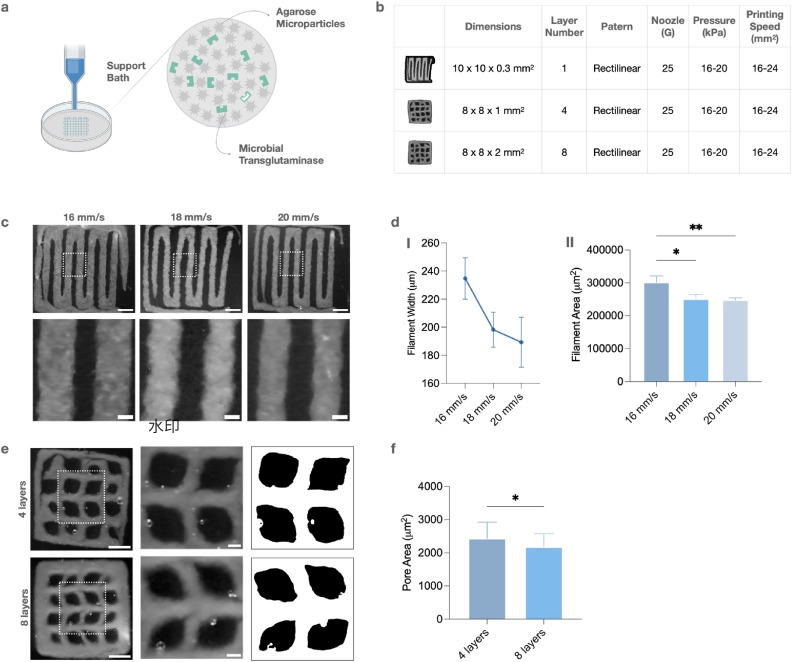
图4. DKECM生物墨水的可打印性与结构稳定性评估
(点击图片查看大图)
最后,研究团队将荧光标记的EVs包载于DKECM生物墨水中进行打印,并评估其释放与摄取行为。结果显示,EVs在构建体中均匀分布,释放呈现两相特征:前48小时释放较快(约75%),随后进入持续缓慢释放阶段,至第14天基本完全释放。从构建体中释放出的EVs仍能被HK-2细胞摄取,定位于细胞核周区域,表明其结构完整性与生物活性得以保持。(图5)
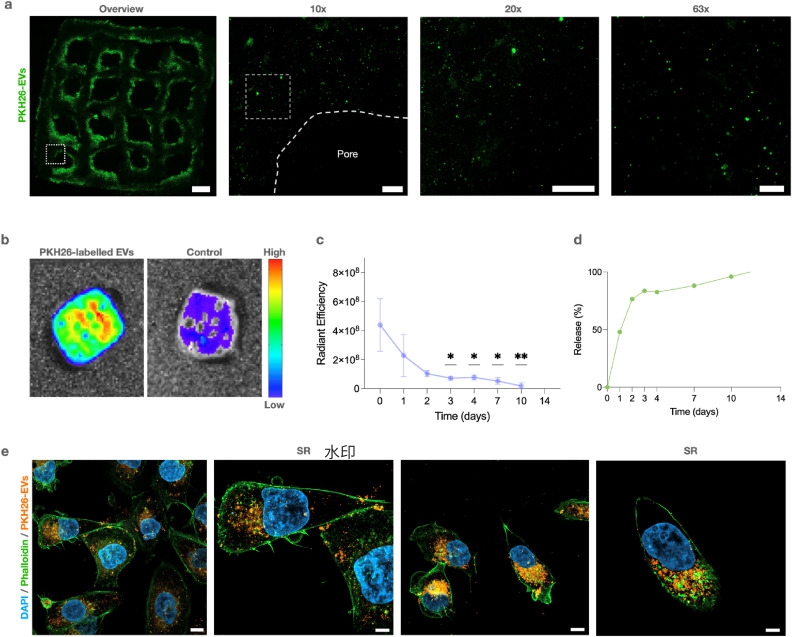
图5. DKECM生物墨水构建体中EVs的持续释放与细胞摄取
(点击图片查看大图)
总结与展望
在该研究中,作者构建了一种完全由肾脏脱细胞基质组成的生物墨水体系,用于肾祖细胞来源EVs的3D生物打印与持续递送,旨在促进肾脏修复。该生物墨水保留了肾脏特异性的基质成分,具备可打印性和控释能力。RPCs来源的EVs在体外能够缓解缺氧引起的过度增殖、氧化应激和损伤相关基因表达,且释放后的EVs仍能被靶细胞摄取。目前该研究仍处于体外阶段,后续需通过体内模型进一步验证其肾脏修复效果。未来,该平台有望拓展至其他器官的再生修复研究。
参考文献:
Quinteira R, Gimondi S, Melica ME, Caballero D, Castanheira A, Espiña B, Lasagni L, Romagnani P, Reis RL, Neves NM. 3D bioprinting meets nanotherapeutics: a vehicle for sustained extracellular vesicle delivery. Biomaterials. 2026 May;328:123851. doi: 10.1016/j.biomaterials.2025.123851.