
导语 狼疮肾炎是系统性红斑狼疮最常见且最严重的器官表现之一,也是导致患者死亡的主要原因。当前标准治疗包括糖皮质激素、免疫抑制剂及生物制剂,但仍有约三分之一的患者会复发,部分最终进展为终末期肾病。本文聚焦于BCMA(B细胞成熟抗原)靶向CAR-T(嵌合抗原受体T细胞)细胞疗法——一种通过基因工程改造、靶向BCMA的自体T细胞产品。一项单臂、开放标签的Ⅰ期临床试验显示,7例难治性狼疮肾炎患者接受单次输注后,疾病活动度评分从中位18分降至0分,5例达到完全缓解,且仅发生1例1级细胞因子释放综合征,未出现神经毒性或严重感染。该研究为BCMA靶向CAR-T疗法在狼疮肾炎中的应用提供了初步循证医学证据,提示其有望成为难治性患者的新治疗选择。
01 研究背景与目的 在狼疮肾炎治疗中,霉酚酸酯、钙调磷酸酶抑制剂及抗CD20单抗等药物虽已取得一定进展,但患者复发风险仍然存在,约5%-30%进展至终末期肾病,提示需要更有效的肾功能保护策略。 狼疮肾炎的核心机制是自身反应性B细胞分化为抗体分泌细胞(浆母细胞和浆细胞),产生大量致病性自身抗体,形成免疫复合物沉积于肾组织。这些细胞多低表达或不表达CD20,且主要位于骨髓或炎症组织,传统抗CD20生物制剂难以有效清除。BCMA表达于浆母细胞、浆细胞及部分记忆B细胞表面,是一个具有潜力的治疗靶点。 本研究通过一项单臂、开放标签的Ⅰ期临床试验,在难治性狼疮肾炎患者中评估BCMA靶向CAR-T细胞疗法的安全性及其诱导疾病缓解的疗效。
02 研究设计 本研究为一项研究者发起的、开放标签、单臂临床试验(注册编号:NCT06277427、NCT06497387),旨在评估BCMA靶向CAR-T细胞在难治性狼疮肾炎患者中的安全性与疗效。 入组标准包括:年龄18-70岁,符合2019年EULAR(欧洲抗风湿病联盟)/ACR(美国风湿病学会)系统性红斑狼疮分类标准,经肾活检证实为活动性增殖性狼疮肾炎(Ⅲ-Ⅴ型),且对多种治疗(糖皮质激素联合≥2种免疫抑制剂或生物制剂)应答不佳。排除标准包括:妊娠或哺乳期、严重肾外表现(如狼疮脑病、肺出血等)、5年内恶性肿瘤史、活动性感染等。 研究共纳入7例经肾活检确诊的难治性狼疮肾炎受试者,中位随访时间为9个月。BCMA CAR-T细胞为每例受试者个体化制备,CAR结构包含人源化抗BCMA单域抗体、CD8α铰链及跨膜区、4-1BB共刺激域和CD3ζ激活域。 (点击图片可查看大图) 图1.入组患者在筛查前的用药信息、治疗过程及随访安排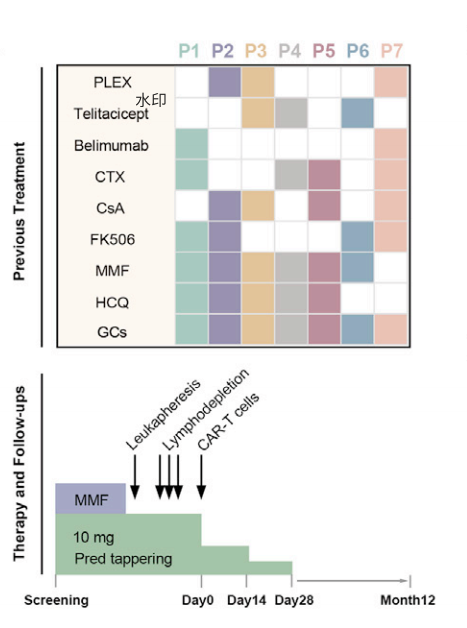
受试者在CAR-T细胞输注前接受氟达拉滨(25 mg/m²/d)和环磷酰胺(300 mg/m²/d)连续3天的淋巴细胞清除化疗。所有受试者接受单次CAR-T细胞输注(2.5×10⁶ cells/kg或3.5×10⁷ cells)。输注前糖皮质激素减量至≤10 mg/天泼尼松,输注后1个月内逐步停用。 随访最长至输注后12个月。主要终点为安全性和不良事件发生率;次要终点为疗效指标(SLEDAI-2K评分、PGA评分、FACIT-F评分等);探索性终点包括自身抗体水平、肾功能、免疫球蛋白及补体水平变化。
03 研究结果 疗效方面,7例受试者SLEDAI-2K(系统性红斑狼疮疾病活动指数2000)评分从中位18分降至0分,PGA(医生整体评估)评分从2.5分降至0分,FACIT-F(慢性病治疗功能评估-疲劳量表)评分从28分升至44分。5例受试者达到DORIS(狼疮缓解定义工作组,)完全缓解标准,全部7例在输注后6个月达到狼疮低疾病活动状态。患者1、2、5分别实现无药物缓解并维持至第12、12、9个月。患者3和患者7的24小时尿蛋白分别从12.21 g降至2.79 g(第9个月)、从7.03 g降至2.39 g(第6个月)。所有受试者免疫球蛋白及自身抗体水平显著下降,补体回升;患者2重复肾活检示免疫复合物沉积显著减少。 安全性方面,未发生神经毒性或CAR-T相关严重感染,仅1例1级细胞因子释放综合征。6例出现<38°C短暂发热,1例38-39.5°C发热,均经物理降温或NSAIDs(非甾体抗炎药)控制。化疗相关血液学毒性4周内恢复。全部7例出现低丙种球蛋白血症,5例接受IVIG(静脉注射免疫球蛋白)补充。多数患者病原体特异性抗体水平下降,但患者3感染COVID-19(新型冠状病毒感染)时抗体滴度较基线升高。 (点击图片可查看大图) 图2. BCMA CAR-T 细胞疗法治疗难治性狼疮性肾炎(LN)的疗效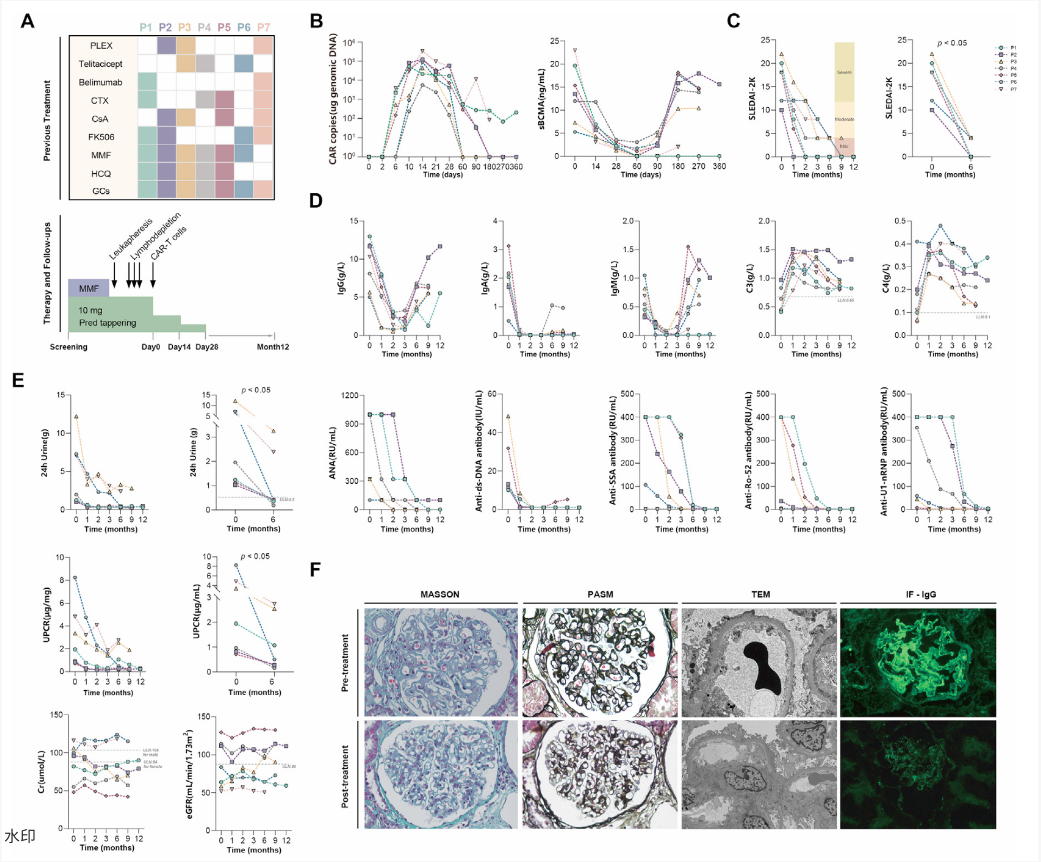
(点击图片可查看大图) 图3.狼疮性肾炎中 BCMA CAR-T 细胞治疗的短期安全性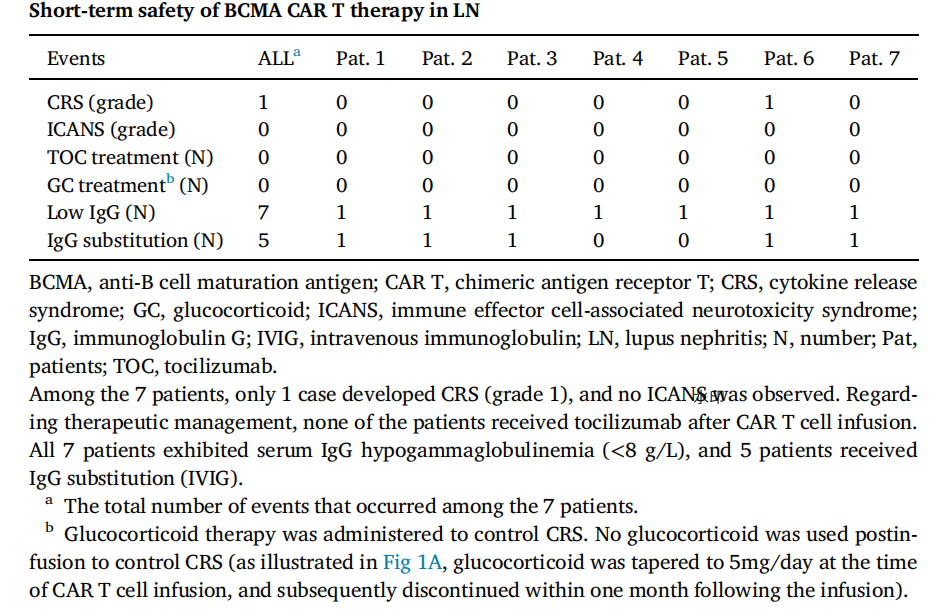
(点击图片可查看大图) 图4.狼疮性肾炎中 BCMA CAR-T 细胞治疗的整体安全性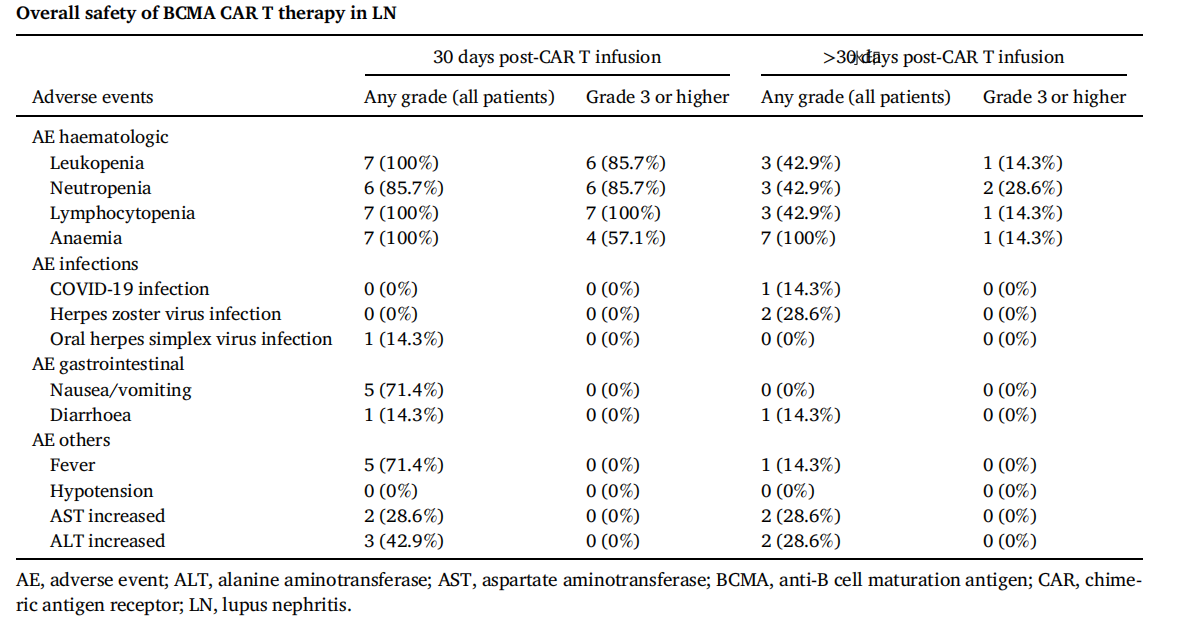
B细胞动态显示,输注后1个月内B细胞完全清除,5例在3个月内恢复正常,重建后以初始B细胞为主(>90%)。单细胞测序(患者3)显示,输注后第3个月B/T细胞受体克隆丰度及多样性降低,促炎信号通路评分显著下降。 (点击图片可查看大图) 图5.BCMA CAR-T细胞治疗期间外周淋巴细胞(尤其是B细胞)的动态变化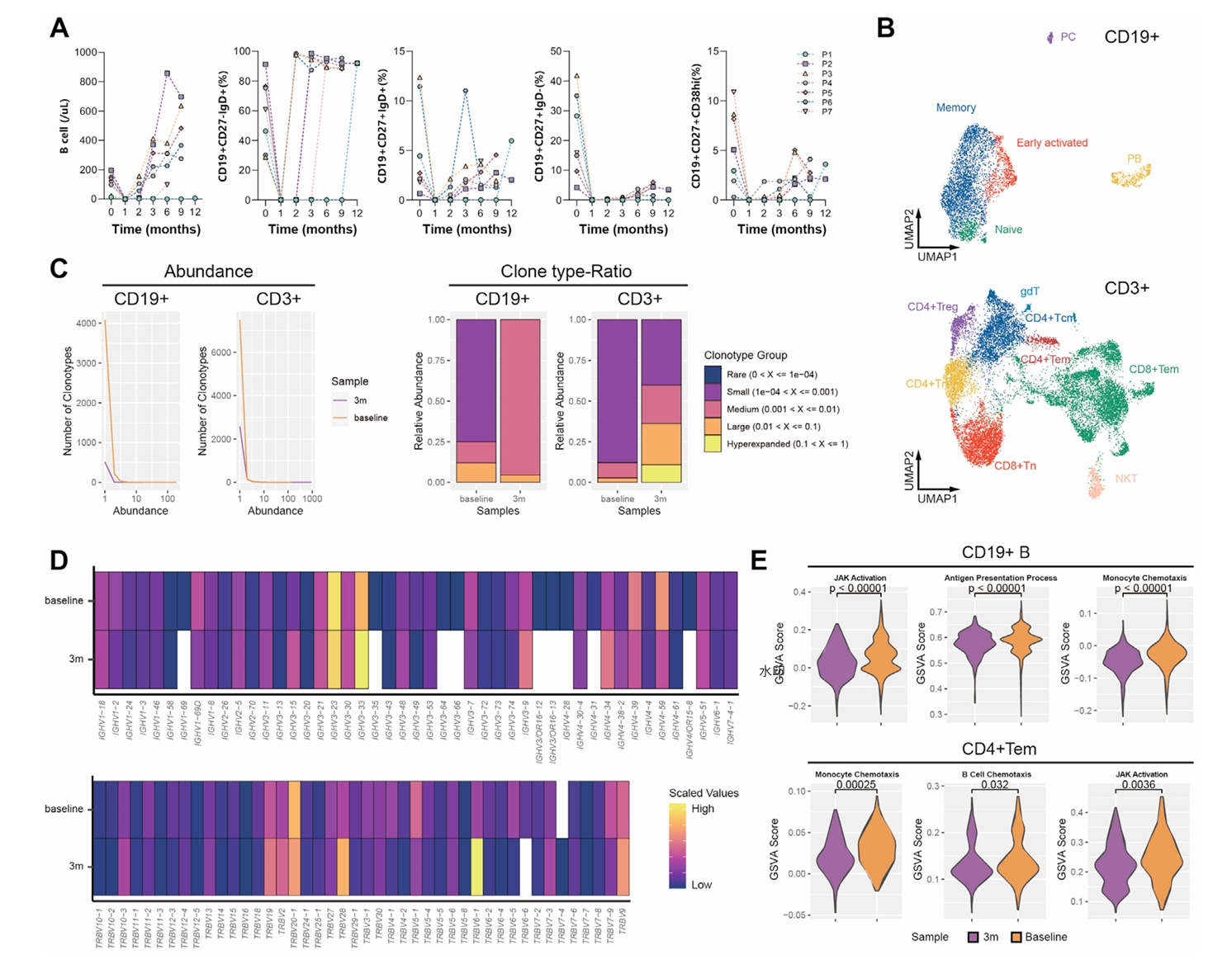
04 研究结论 本研究表明,BCMA靶向CAR-T细胞疗法可有效清除狼疮肾炎患者的外周B细胞,促进免疫重建,并安全、有效地诱导无药物缓解。该疗法为难治性狼疮肾炎患者提供了新的治疗选择,同时也提示单纯BCMA靶向策略在治疗以异常体液免疫应答为特征的自身免疫性疾病中具有可行性。
结语 在现有标准治疗基础上,难治性狼疮肾炎患者仍存在疾病复发和进展至终末期肾病的风险。BCMA靶向CAR-T细胞疗法通过靶向表达BCMA的浆母细胞、浆细胞及部分记忆B细胞,为这一临床问题提供了新的干预策略。本项Ⅰ期临床试验显示,7例难治性患者接受单次输注后,疾病活动度改善,5例达到完全缓解,发生1例1级细胞因子释放综合征,未出现神经毒性或严重感染。与抗CD19 CAR-T和CD19/BCMA双靶向策略相比,单纯BCMA靶向可能实现范围更窄的B细胞清除,在保留部分B细胞免疫功能的同时可能降低感染风险。该研究为BCMA靶向CAR-T疗法在狼疮肾炎中的应用提供了初步依据,其临床价值需要更大样本量和更长随访时间的研究进一步验证。
参考文献:
Ziwei Hu, et al."BCMA-targeted CAR T cell therapy can effectively induce disease remission in refractory lupus nephritis.."Annals of the rheumatic diseases 84.10(2025):1675-1683.doi:10.1016/J.ARD.2025.06.2128.