
慢性肾病是导致发病率和死亡率的重要原因,截至2022年影响美国约14%的成年人口,80万患者需要肾替代治疗。目前肾脏移植面临供体短缺和免疫排斥等问题,移植肾即使使用免疫抑制剂平均寿命也仅约12年。诱导多能干细胞(iPSCs)可分化为肾脏类器官,但最佳植入阶段尚不明确:成熟类器官结构完整但植入后易退化,早期祖细胞潜力巨大但具体窗口期不清楚。
近期,华盛顿大学Benjamin S. Freedman团队和以色列Sheba医学中心Benjamin Dekel团队在《The Innovation》(IF 25.7)发表题为"Co-induction of stromal and epithelial progenitors for renal regeneration"的研究。该研究比较了不同分化阶段iPSC衍生肾脏细胞的植入效果,发现早期诱导后肾间充质(iMM)优于成熟类器官,并揭示了iMM通过协同诱导肾单位和间质祖细胞促进血管化肾单位形成的机制。
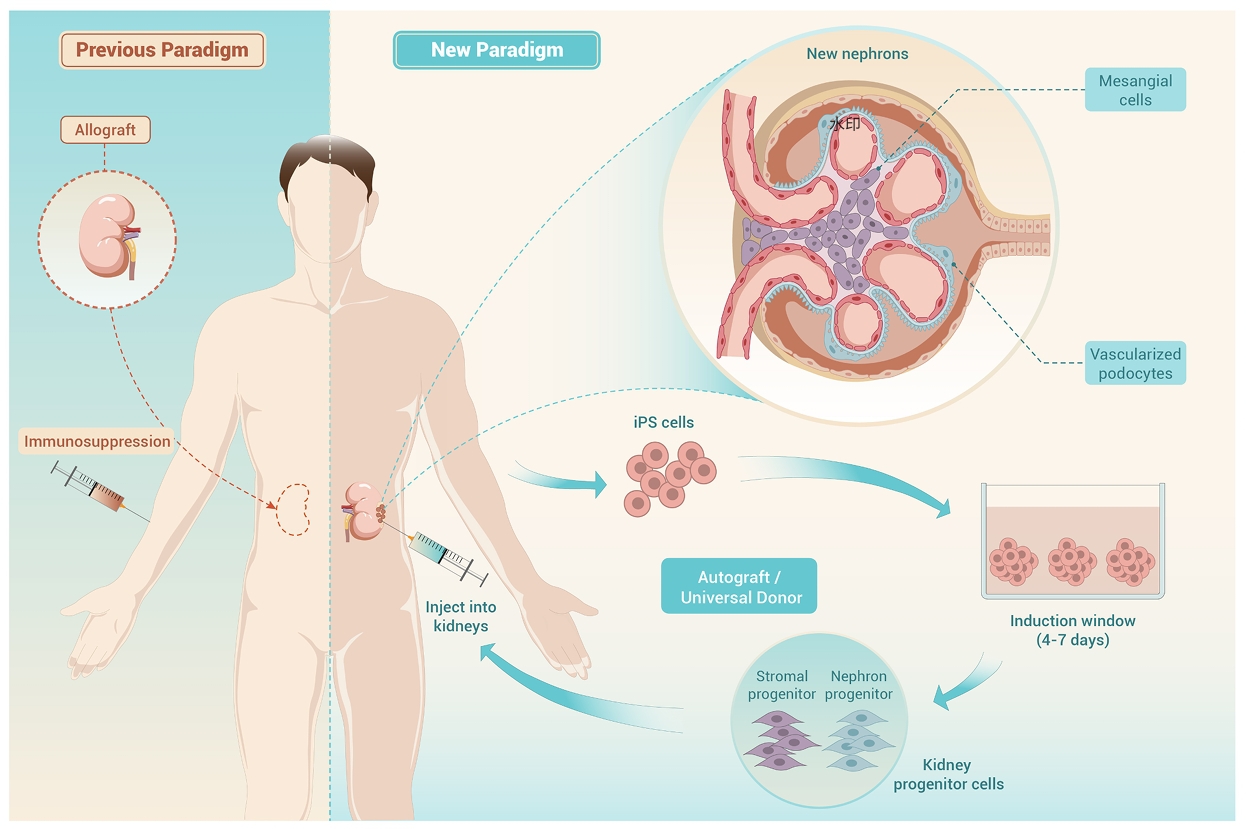
图形摘要
研究内容
研究团队首先通过时间序列分析明确了iPSC向肾脏细胞分化的动态过程(图1)。采用CHIR99021脉冲诱导后,在分化第0–6天连续取样进行qPCR和免疫荧光检测,结果显示细胞经历了一个典型的发育阶段转换:早期(第0–3天)首先上调中间中胚层标志物PAX2和OSR1;随后在第4–6天,肾后肾间充质相关标志物显著升高,包括肾间充质(SALL1、SIX1)、肾单位祖细胞(SIX2、ITGA8)以及肾间质祖细胞(PDGFRα);而在第7天之后,上皮化及肾单位各节段分化标志物逐渐表达,提示细胞开始向成熟结构分化。RNA测序进一步证实,第7天细胞群体富集肾单位祖细胞和肾间质祖细胞特征。基于这一连续变化过程,研究团队确定第4–7天为关键“移植窗口期”,此时细胞处于诱导后肾间充质(iMM)阶段,兼具两类前体细胞特性,具有最佳的体内发育潜能。
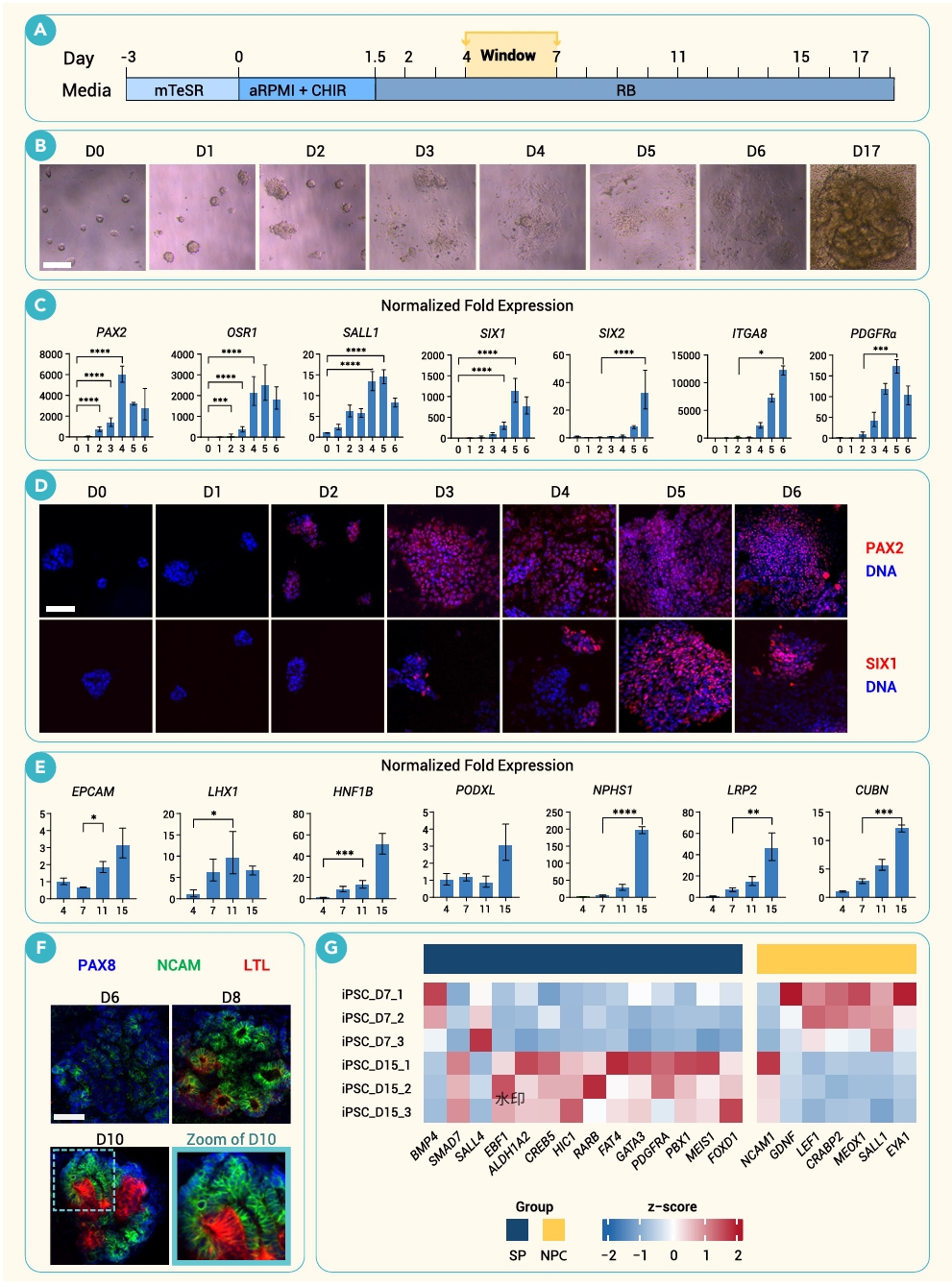
图1. 细胞标记的时间变化显示了移植的最佳窗口期
(点击图片查看大图)
在此基础上,研究团队比较了第7天的iMM与第15天成熟类器官的移植效果(图2),发现两者差异显著:将其分别移植至小鼠肾被膜下21天后,iMM组能够形成大量肾单位结构,包括足细胞(hPODXL⁺)和近端小管(LTL⁺)(约1.98和8.07个/mm²),而成熟类器官组则几乎完全无法形成这些结构(均为0)。进一步的时间动态分析显示,成熟类器官移植后仅3天即出现囊肿,随后肾小球和小管结构逐渐退化,尽管移植物体积增加,但属于无序增殖;相比之下,iMM移植后持续分化并维持稳定的肾单位结构,甚至在29天后仍保持完整。这表明,处于早期前体状态的iMM具有更强的可塑性和体内发育潜能,而过度分化的成熟类器官反而失去整合能力,提示肾脏再生存在一个关键的“最佳移植窗口期”。
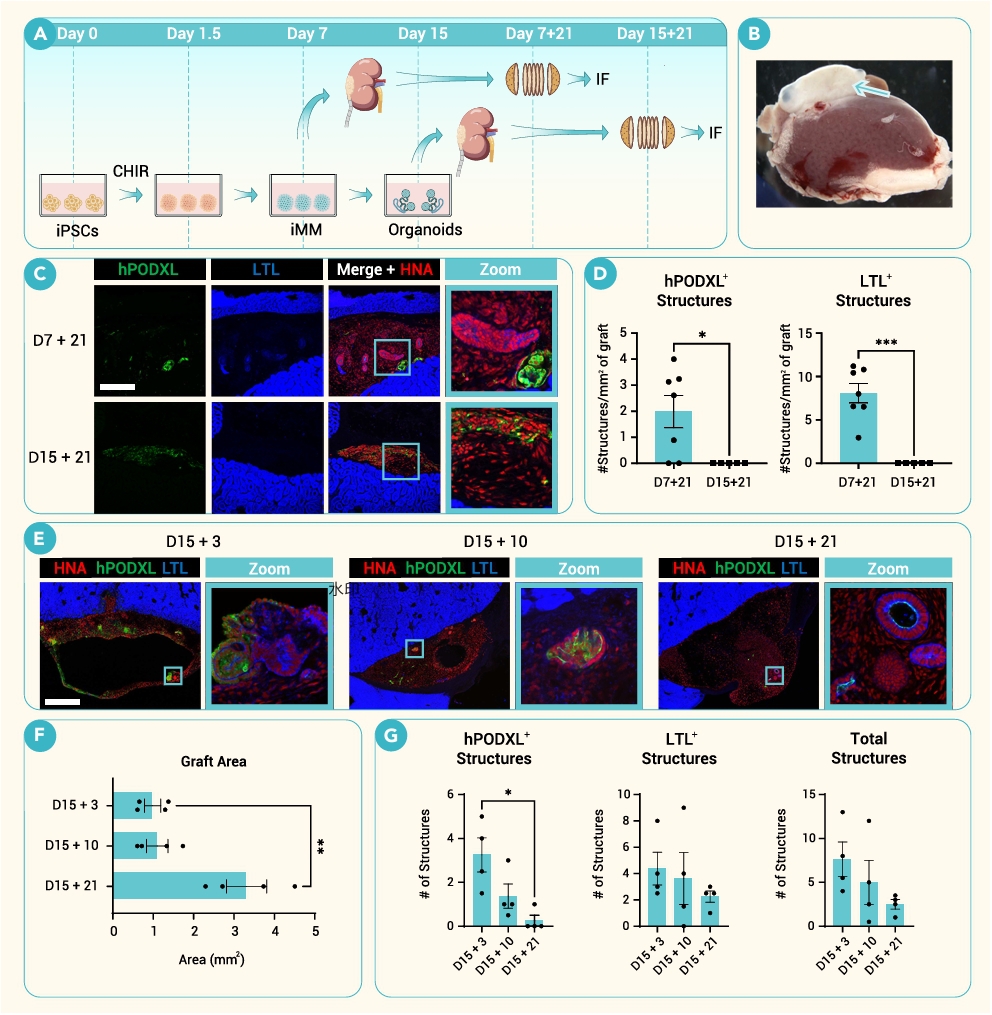
图2. iMM(早期前体细胞)在移植形成方面优于成熟类器官
(点击图片查看大图)
研究团队进一步解析了研究团队进一步解析了iMM在体内形成肾单位的细胞组成及其结构成熟度(图3)。免疫荧光结果显示,人源足细胞(hPODXL⁺)和壁层上皮细胞(PAX8⁺)包裹着宿主小鼠来源的血管内皮细胞(mCD31⁺),共同构建出一种“人-鼠嵌合”的肾小球结构;同时首次观察到GATA3⁺/HNA⁺人源系膜细胞分布于毛细血管袢之间并表达PDGFRB,提示iMM来源的肾间质祖细胞在体内成功分化并补全肾小球的关键组成部分。电镜进一步证实毛细血管内存在红细胞、足细胞与内皮之间形成基底膜并表达PV1,说明该结构已具备初步滤过功能;此外,第4天iMM同样可以形成分段的肾单位,且肾小管密度甚至高于第7天,但肾小球成熟度略低;同时qPCR显示FOXD1在第5天显著上调,进一步证明体系中存在并诱导了肾间质祖细胞的分化。
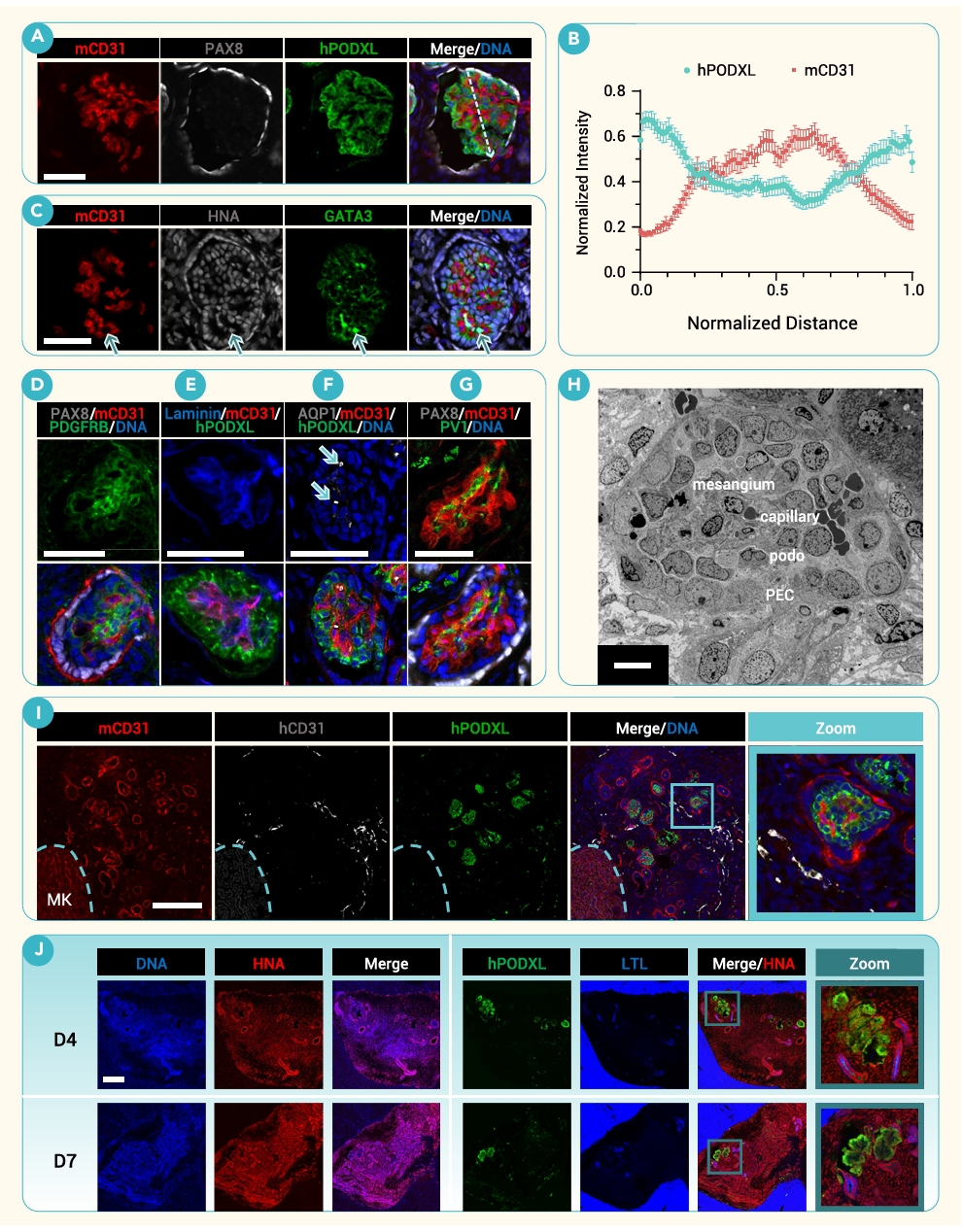
图3. 移植的人类足细胞和系膜细胞招募小鼠内皮细胞形成肾小球
(点击图片查看大图)
最后,研究团队比较了体外培养与体内移植对肾小管成熟度的影响(图4)。结果显示,与体外培养21天的类器官相比,移植到小鼠体内21天的iMM来源移植组织中,近端小管标记AQP1、髓袢标记UMOD和远端小管标记GATA3的表达均显著升高,说明体内环境明显促进了肾小管分化成熟。电镜进一步显示,这些肾小管具有丰富线粒体和完整的顶端结构,提示其已具备较强的物质转运能力;同时,宿主血管侵入并形成PV1⁺的周小管毛细血管网络,紧密环绕PAX8⁺肾小管,提供血供支持。此外,MEIS1⁺/PDGFRB⁺肾间质细胞分布在小管周围,形成类似体内的间质微环境。整体来看,这些结果表明,iMM在体内不仅能够形成结构完整的肾单位,还能实现体外类器官难以达到的成熟度和血管化水平。
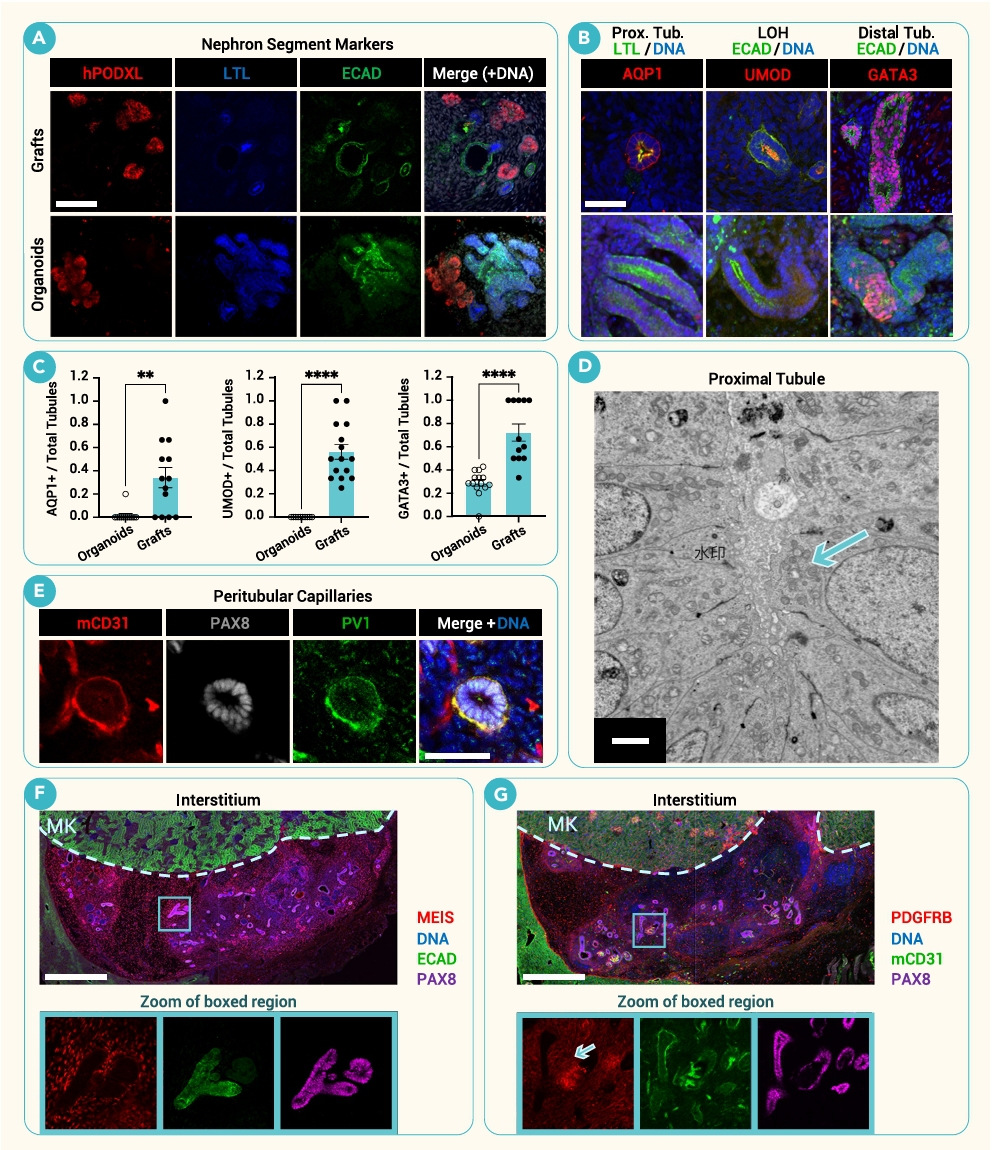
图4. 移植的小管比体外类器官更成熟
(点击图片查看大图)
总结与展望
本研究表明,iPSC衍生肾脏细胞在不同分化阶段具有显著不同的体内发育潜能,其中第4–7天的诱导后肾间充质(iMM)为最佳移植窗口。该阶段细胞同时具备肾单位祖细胞和肾间质祖细胞特性,可在体内形成完整肾单位并招募宿主血管,实现较高成熟度;而成熟类器官移植后则发生退化,难以维持结构。上述结果提示,细胞分化阶段是影响体内整合与结构重建的关键因素。未来需进一步评估其功能修复效果并优化移植条件,同时提升组织成熟度与长期稳定性,为基于发育阶段调控的肾脏再生策略提供参考。
参考文献:
Vincent T, Nademi S, Namestnikov M, Cohen-Zontag O, Dekel B, Freedman BS. Co-induction of stromal and epithelial progenitors for renal regeneration. The Innovation. 2026;7(5):101281. DOI: 10.1016/j.xinn.2026.101281