
急性肾损伤(AKI)和慢性肾病(CKD)是全球范围内高发病率和高死亡率的疾病,目前临床上仍缺乏能够有效修复受损肾脏、逆转疾病进程的治疗手段。尽管基于干细胞的再生医学策略备受关注,但人诱导多能干细胞来源的肾祖细胞(hiPSC-NPCs)的临床应用面临两大瓶颈:缺乏高效扩增方法以及细胞异质性高。
2025年4月,日本京都大学Osafune Kenji(长船健二)团队在 Science Translational Medicine 上发表题为“Human iPSC-derived nephron progenitor cells treat acute kidney injury and chronic kidney disease in mouse models”的文章。该研究开发了一种高效扩增人诱导多能干细胞衍生肾祖细胞(hiPSC-NPCs)的方法,验证了其在治疗急性肾损伤(AKI)和慢性肾病(CKD)中的疗效,并揭示了其通过分泌VEGF-A发挥作用的核心机制。
研究内容
为探究hiPSC-NPCs的治疗潜力,研究团队首先验证了其分化潜能。体外实验显示,hiPSC-NPCs能够形成肾脏类器官,表达足细胞(PODXL⁺)、近端小管(LTL⁺)和远端小管(CDH1⁺)的标志物,表明其具备向肾单位各组分分化的能力。在此基础上,团队进一步评估了hiPSC-NPCs对AKI的治疗效果。将未诱导分化的hiPSC-NPCs移植至顺铂诱导的AKI小鼠肾被膜下,结果显示移植组小鼠血尿素氮(BUN)和血清肌酐(S-Cre)显著降低,肾小管坏死、管型形成等病理损伤减轻,生存率从对照组的31.7%提高至85%以上。相比之下,经过体外诱导分化2天的hiPSC-FS-NPCs移植后治疗效果较弱。这一结果表明,hiPSC-NPCs在不分化为肾脏类器官时可能具有更强的治疗潜力。
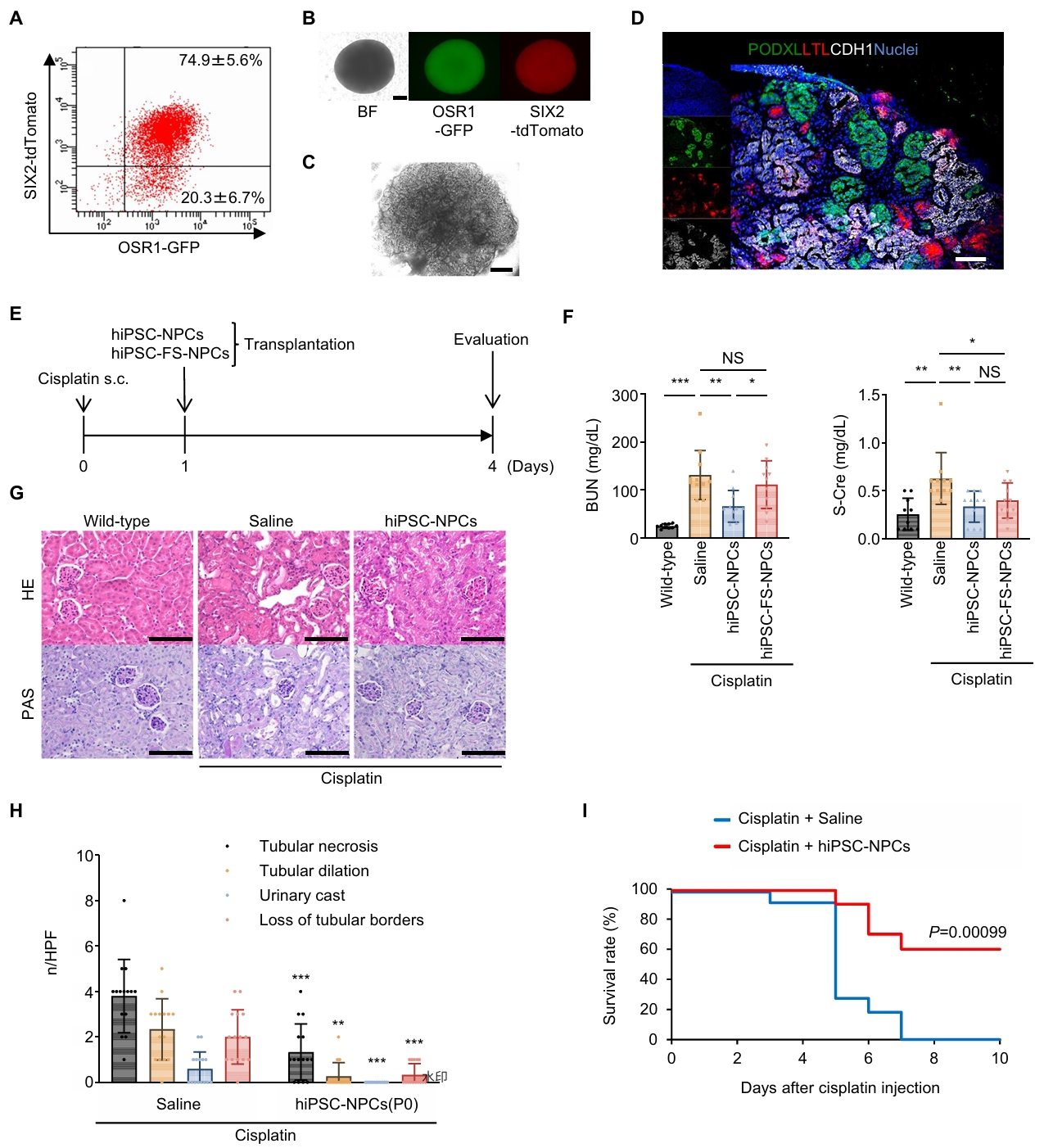
图1. 未诱导分化为肾脏类器官的hiPSC-NPCs对顺铂诱导的AKI小鼠具有治疗效果
(点击图片查看大图)
为实现hiPSC-NPCs的高效扩增,研究团队开发了CFY培养基(含CHIR99021、FGF9和Y-27632),并结合悬浮聚集体培养体系。结果显示,hiPSC-NPCs在CFY培养基中经两次传代后增殖超过100倍,OSR1、SIX2、PAX2等NPC标志物表达稳定维持,且传代后的细胞仍能分化为包含足细胞、近端小管和远端小管的肾单位类器官。该培养基适用于多个hiPSC系,具有良好的普适性。进一步将扩增后的hiPSC-NPCs(传代1次P1、传代2次P2)移植至AKI小鼠,结果显示P1和P2组均能有效改善肾功能、减轻组织损伤并提高生存率,且P2组疗效优于P1组,提示多次传代后的细胞仍保持治疗效果。
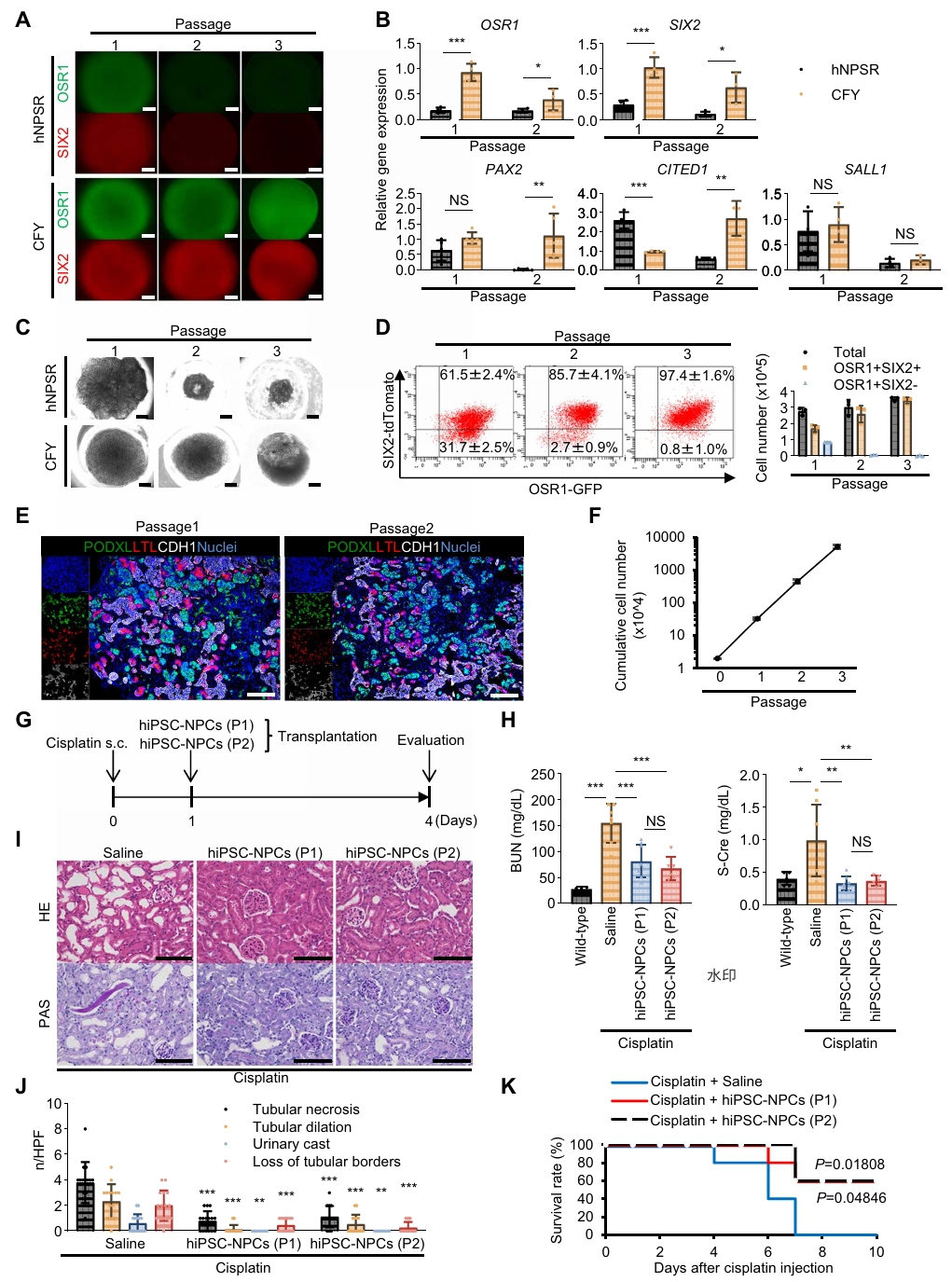
图2. 扩增后的hiPSC-NPCs改善顺铂诱导的AKI小鼠肾损伤与生存率
(点击图片查看大图)
随后,研究团队进一步评估了hiPSC-NPCs对CKD的治疗效果。在马兜铃酸诱导的CKD小鼠模型中,将未诱导分化的hiPSC-NPCs移植至肾被膜下,结果显示移植组小鼠肾功能显著改善(BUN、S-Cre和尿蛋白水平降低),肾间质纤维化明显减轻(胶原沉积和肌成纤维细胞活化减少),且肾脏衰老得到有效延缓(SA-β-Gal活性及相关基因表达降低)。
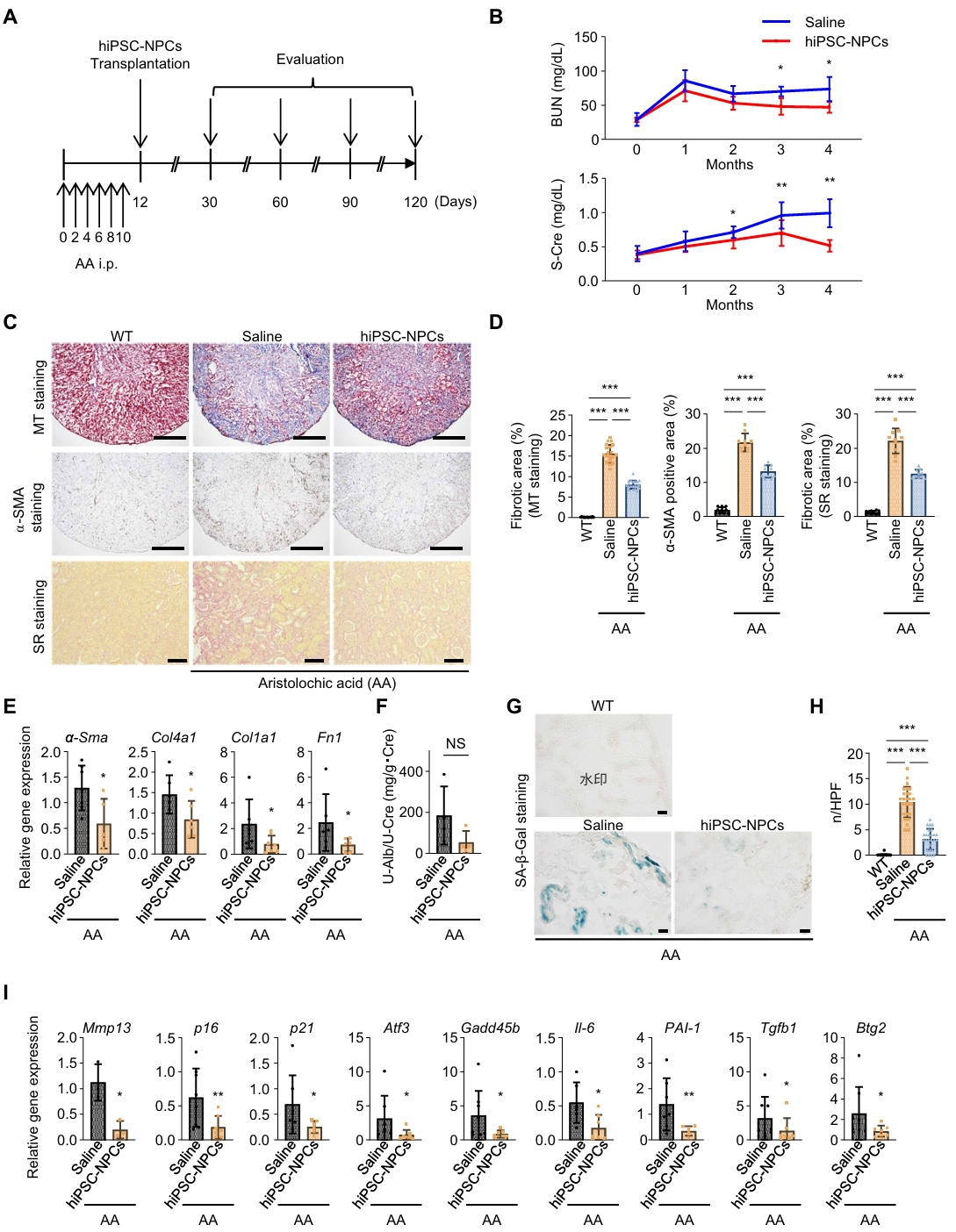
图3. hiPSC-NPCs移植改善CKD小鼠肾功能、减轻纤维化并延缓衰老
(点击图片查看大图)
为探究hiPSC-NPCs的作用机制,研究团队首先证实移植的细胞并未整合入宿主肾脏,提示其治疗作用依赖于旁分泌途径。在此基础上,团队构建了巨型细胞聚集体并收集其条件培养基(CM)。将CM腹腔注射至AKI小鼠,结果显示CM能显著改善肾功能、减轻肾小管损伤并提高生存率,且冷冻保存后的CM仍保留疗效。这一结果表明,hiPSC-NPCs通过分泌因子发挥治疗作用,而非依赖细胞整合,提示CM可作为“无细胞治疗”策略。
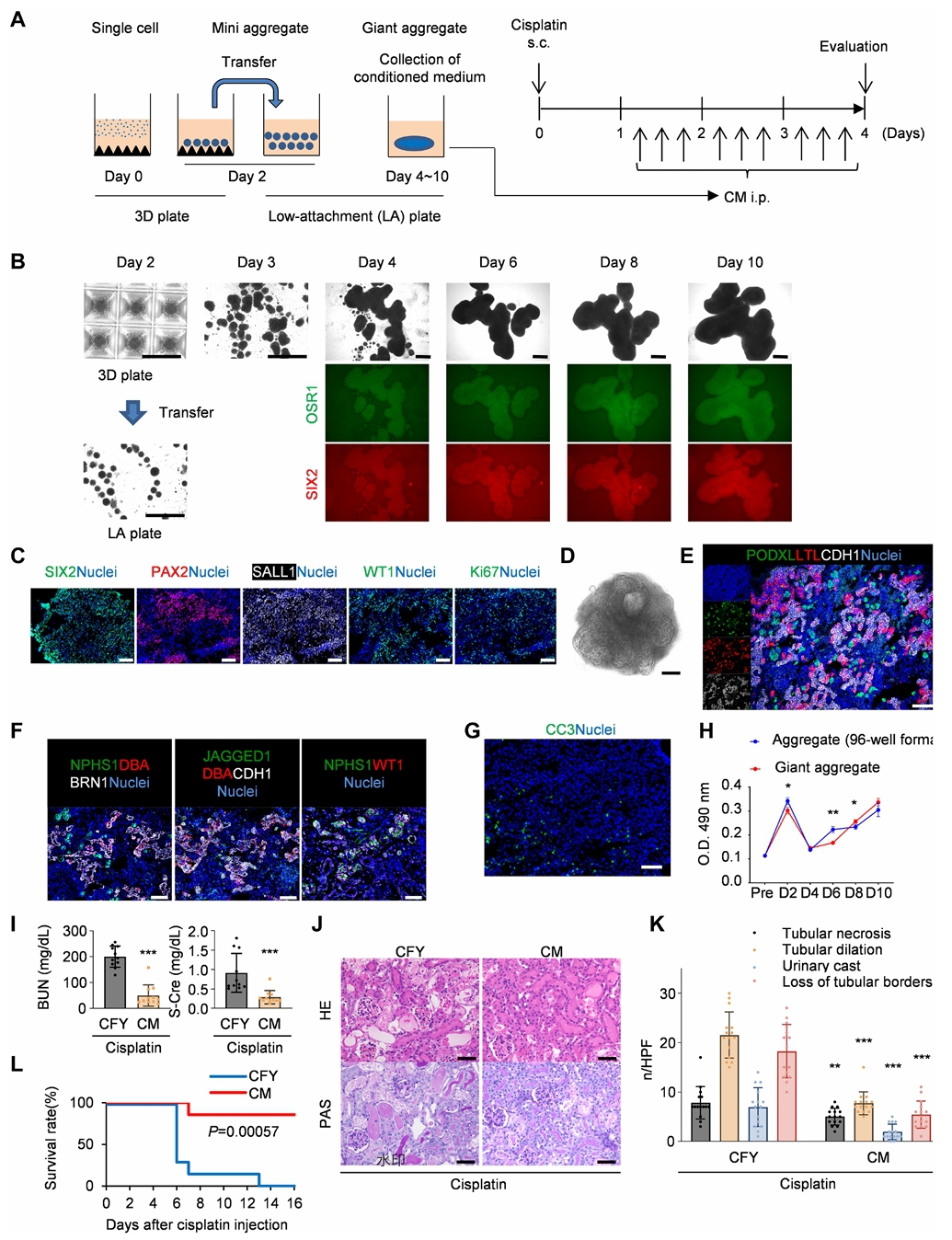
图4. 巨型hiPSC-NPC聚集体来源的条件培养基(CM)改善AKI小鼠肾损伤
(点击图片查看大图)
随后,为明确hiPSC-NPCs分泌的关键效应分子,研究团队通过RNA-seq分析发现hiPSC-NPCs高表达VEGF-A。将重组VEGF165蛋白局部缓释至AKI小鼠肾被膜下,结果显示VEGF-A能够增加肾微血管密度、减少凋亡细胞,从而改善肾功能。这些结果支持VEGF-A作为hiPSC-NPCs治疗AKI的关键机制之一。
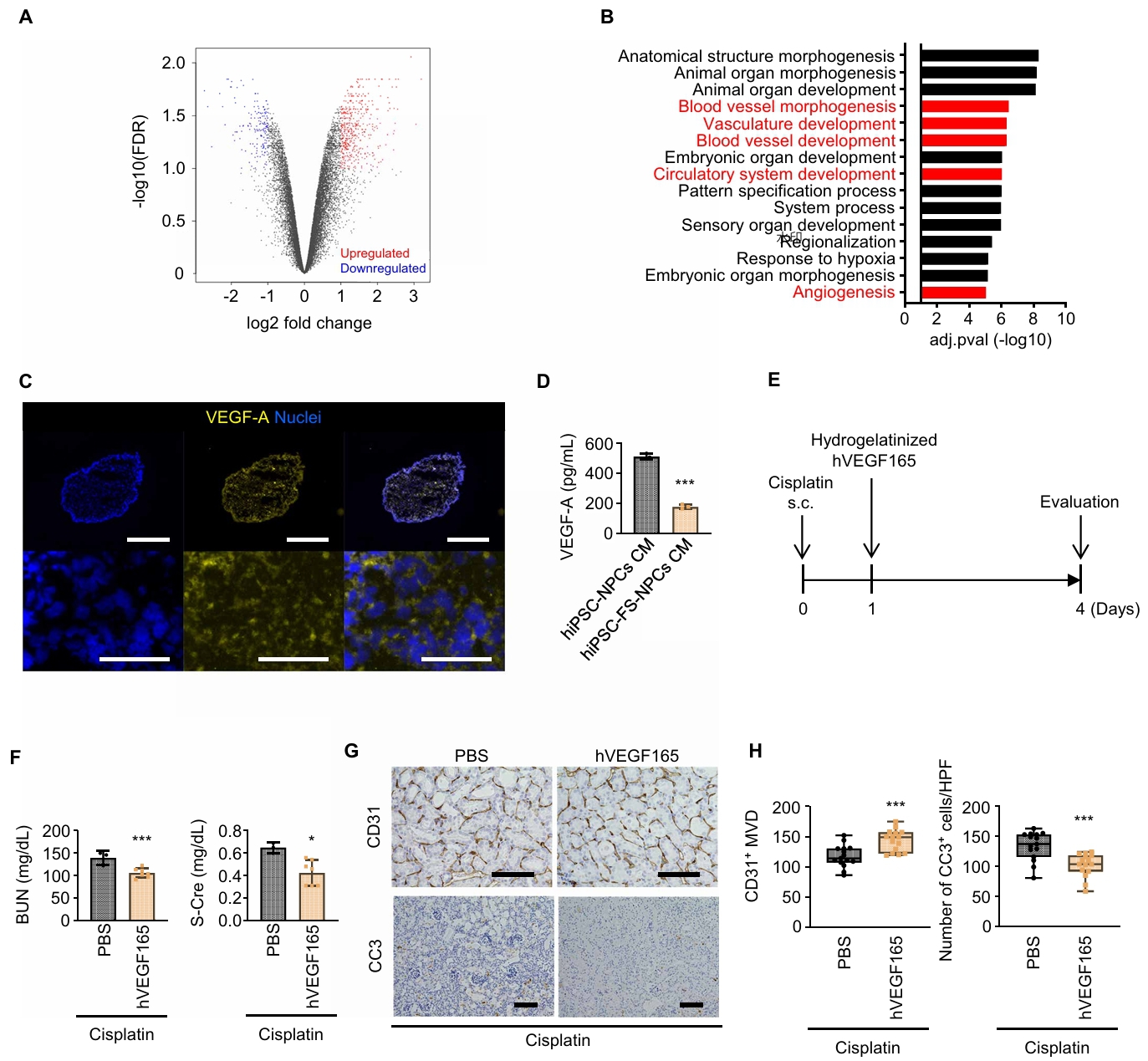
图5. hiPSC-NPCs治疗AKI的机制涉及VEGF-A介导的血管生成
(点击图片查看大图)
最后,为验证VEGF-A在hiPSC-NPCs治疗中的关键作用,研究团队利用CRISPR-Cas9系统构建了VEGFA基因敲除的hiPSC-NPCs。将VEGFA KO hiPSC-NPCs分别移植至AKI和CKD小鼠模型,结果显示KO组在改善肾功能、减轻肾损伤和纤维化方面效果均显著降低,而野生型组则保持良好疗效。这些结果表明,VEGF-A在hiPSC-NPCs对AKI和CKD的治疗效果中起着关键作用。
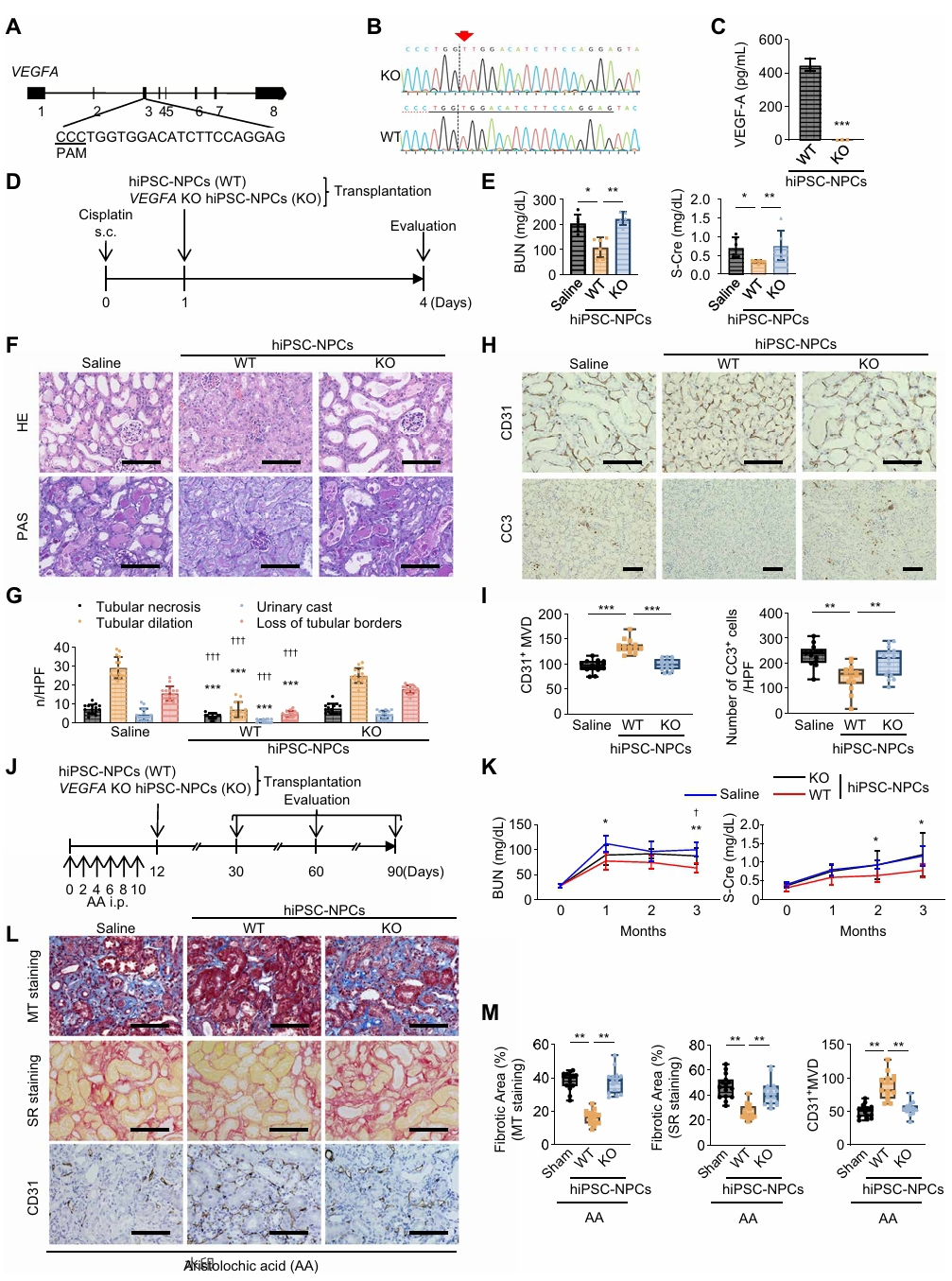
图6. VEGFA基因敲除后hiPSC-NPCs对AKI和CKD模型的治疗效果降低
(点击图片查看大图)
总结与展望
在该研究中,作者揭示了hiPSC-NPCs治疗AKI和CKD的关键机制。具体而言,CFY培养基可实现hiPSC-NPCs超过100倍的高效扩增,c-MET可作为其特异性纯化标志物。hiPSC-NPCs通过分泌VEGF-A促进血管生成、减少细胞凋亡、抑制纤维化并延缓衰老,从而发挥多重保护作用。VEGFA基因敲除实验证实VEGF-A是该治疗策略的核心效应分子。此外,基于条件培养基的“无细胞疗法”可简化操作流程。未来,靶向VEGF-A信号通路、优化免疫兼容性(如HLA匹配iPSCs)以及探索CM成分的药理潜力,有望成为开发肾脏疾病新型治疗策略的重要方向。
参考文献:
Araoka T, Toyohara K, Ryosaka M, Inui C, Matsuura M, Ma C, Watahiki J, Li Z, Iwasaki M, Watanabe A, Yokokawa R, Tabata Y, Izpisua Belmonte JC, Osafune K. Human iPSC-derived nephron progenitor cells treat acute kidney injury and chronic kidney disease in mouse models. Sci Transl Med. 2025 Apr 2;17(792):eadt5553.