当全球7.9亿慢性肾脏病患者的希望从透析机转向实验室,一个关键问题摆在面前:那些年复一年的基础研究,究竟有多少已经转化为可及的治疗方案?
答案指向同一个方向——肾祖细胞(NPC)。这是诺奖级iPS技术在肾脏再生领域最明确的转化路径,也是全球高手同场竞技的赛道。

在日本京都,一家名为Rege Nephro的公司正沿着这条路径稳步前行。梳理它的发展轨迹,或许能让我们更清晰地看到:诺奖级技术加持下的肾脏再生,正在一步步走向临床。
1
临床困境:肾脏再生为何被寄予厚望
慢性肾脏病(CKD)是全球性的公共卫生难题:患者7.9亿,中国1.56亿,仅日本就有1300万,其中34万人依赖透析生存,每年医疗费用高达1.2万亿日元。
更棘手的是临床选择匮乏。现有药物只能延缓病程,无法修复受损组织;终末期患者要么终身透析,生活质量极低,要么等待肾移植,却受限于供体短缺。这片巨大的未满足需求,正是肾脏再生医学的发力点。而日本凭借iPS细胞技术的先发优势,在这一领域持续深耕。
2
技术源头:诺奖级iPS技术催生的“肾脏种子”
任何再生医学产品的起点,都是源头技术的突破。Rege Nephro的技术根基,源自京都大学iPS细胞研究所(CiRA)——山中伸弥教授获得诺贝尔奖的学术圣地。创始人長船健二教授的两项核心突破,打通了肾脏再生的产业化路径:
第一,找到“种子”。在全球率先鉴定出胚胎发育中形成肾单位的源头——肾祖细胞(NPC),明确了应该用哪种细胞去修复肾脏。
第二,学会“播种”。开发出从人类iPS细胞高效诱导高纯度肾祖细胞的独家方案,攻克了肾脏细胞制备的关键瓶颈。
这两项突破构成了Rege Nephro的核心专利壁垒,也让肾祖细胞(NPC)成为iPS技术在肾脏再生领域的重要落点。

图1.京都大学iPS细胞研究所长船健二教授

图2.利用人iPS细胞的慢性肾病细胞疗法
3
研发布局:三条路径并行推进
Rege Nephro的研发管线清晰地分为三个层面:
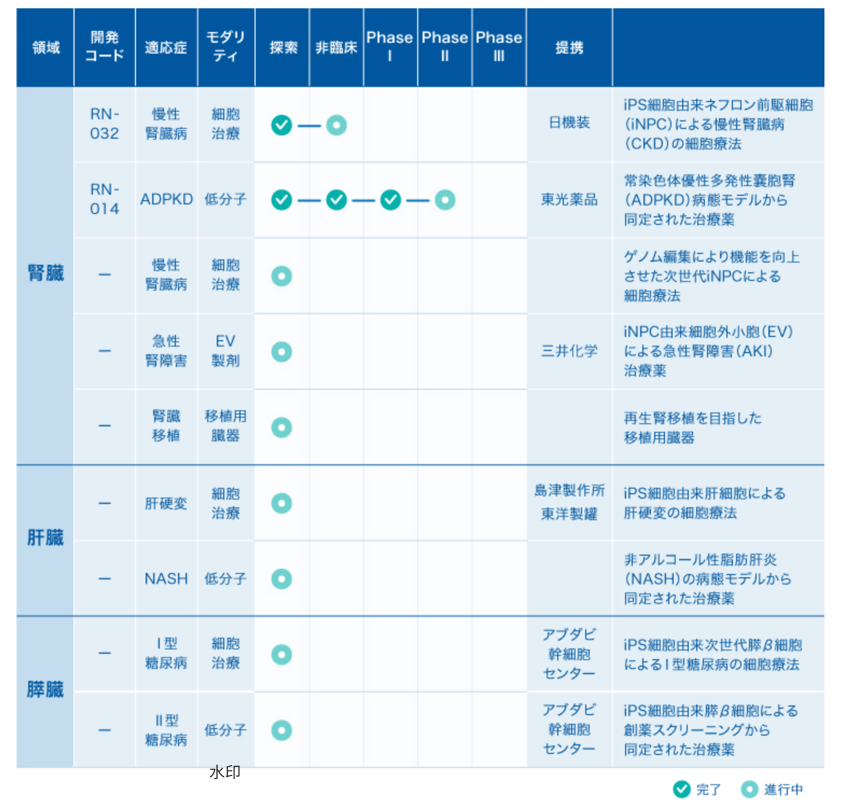
图3. Rege Nephro研发管线
路径一:细胞疗法(RN-032)——以肾祖细胞为核心
这是公司的核心产品,将iPS来源的肾祖细胞移植到肾脏被膜下。这些细胞不会直接再生新肾,而是通过旁分泌效应释放营养和抗炎因子,保护残存肾单位、延缓疾病进展。
给药方式选择肾脏被膜下注射,该部位免疫原性较低,能将细胞局域化,提高安全性。目标患者优先选择肾移植后肾功能衰退的人群——这类患者已使用免疫抑制剂,医疗监测严密,有利于初期安全性验证。
最新进展:目前,该疗法的有效性正在小动物实验中进行验证,生产工艺的开发也在推进中。
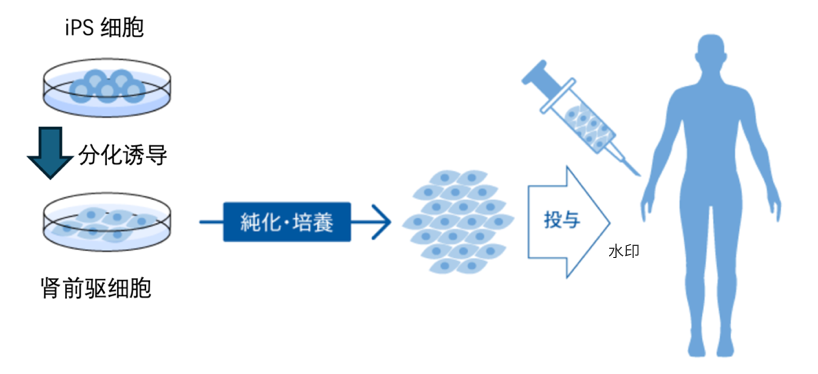
图4. iPS细胞诱导分化为肾祖细胞的技术流程:从人iPS细胞出发,经诱导分化、纯化培养
药效数据:
在顺铂诱导的急性肾损伤(AKI)小鼠模型中,hiPSC来源的肾祖细胞移植可显著改善肾功能:血尿素氮从约200 mg/dL降至约50 mg/dL,血清肌酐从约1.5 mg/dL降至约0.5 mg/dL;组织学损伤减少50%以上;小鼠生存率从31.7%提升至97.4%。
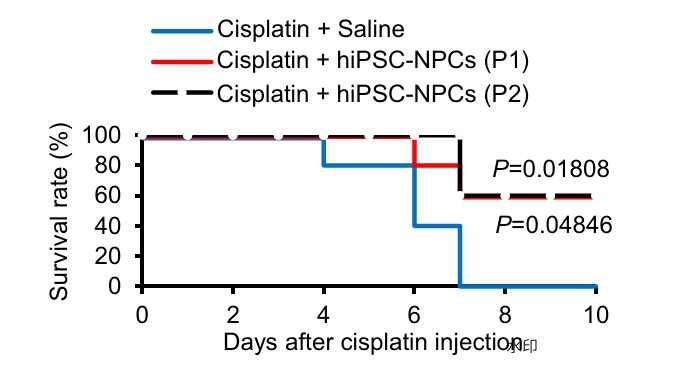
图5. P2组小鼠生存率提高至97.4%,显著高于对照组(31.7%)和P1组(61.5%)
在马兜铃酸诱导的慢性肾病(CKD)小鼠模型中,肾祖细胞移植同样显示出多重保护作用:延缓肾功能恶化,肾间质纤维化面积从约20%降至5%,尿蛋白排泄量降低,肾脏衰老细胞数量减少约67%,并显著抑制炎症和纤维化相关基因表达。
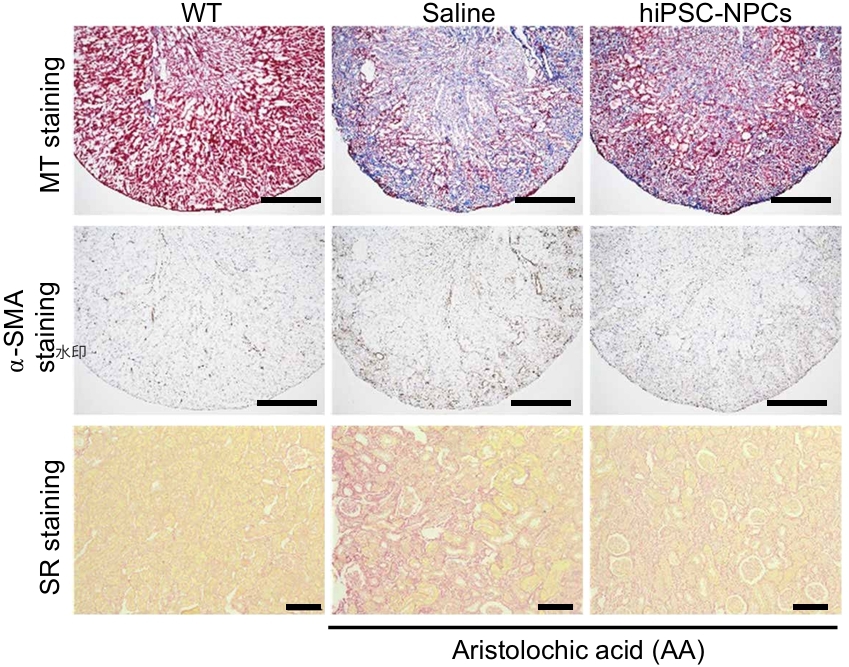
图6. Masson染色(MT):肾间质纤维化面积减少(从约20%降至5%)
作用机制:通过RNA测序和基因敲除实验证实,肾祖细胞主要通过分泌血管内皮生长因子A(VEGF-A)发挥治疗作用,而非直接分化为肾单位细胞整合入宿主肾脏。VEGF-A能够促进血管生成、减少细胞凋亡,从而改善肾功能。
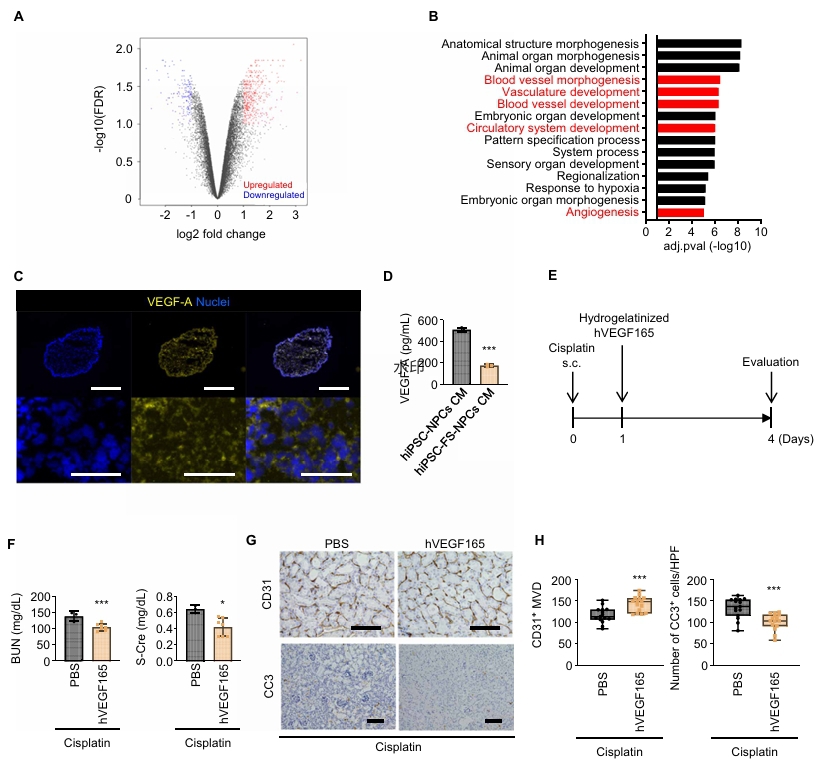
图7. hiPSC-NPCs通过分泌VEGF-A在顺铂诱导的AKI小鼠模型中发挥治疗作用。VEGF-A能够增加肾微血管密度,减少凋亡细胞,从而改善肾功能。这些结果支持VEGF-A作为hiPSC-NPCs治疗AKI的关键机制之一,并为未来的治疗策略提供了潜在的靶点。后获得肾祖细胞,最终用于临床给药
路径二:小分子药物(RN-014)——风险对冲
这是公司最接近商业化的产品,用于治疗常染色体显性多囊肾病——一种全球约1250万人受困的遗传性肾病。RN-014最初由Syros Pharmaceuticals开发,Rege Nephro获得其多囊肾病适应症的权益后,于2023年12月在日本启动二期临床试验。为进一步拓展美国市场,公司于2025年2月从Syros收购了该药物的完整开发资产。
小分子管线的价值在于:开发周期短、成功率高,能为公司提供早期现金流和临床开发经验,同时对冲细胞疗法的高技术风险。
路径三:类器官平台——技术外延
通过构建患者来源的肾脏类器官(“迷你肾脏”),Rege Nephro为制药企业提供药物筛选和毒性测试服务。与阿斯利康的合作,证明这一平台已具备产业价值。
远期愿景:整合多种肾脏前体细胞,在生物支架上构建具有过滤、重吸收功能的三维肾脏组织,代表再生医学的终极方向。
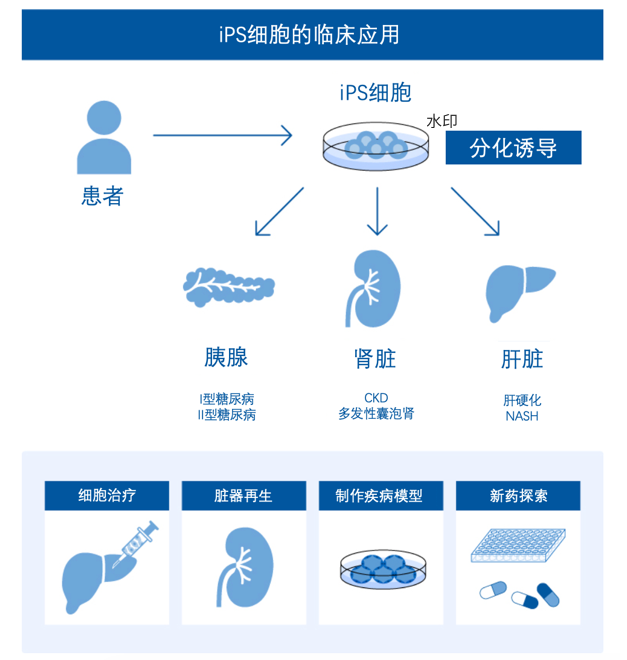
图8. iPS细胞的临床应用
4
商业模式:一家学术衍生公司的生存之道
从京都大学实验室走出的Rege Nephro,其商业化路径有几个值得关注的特点:
第一,源头技术筑底。 長船教授十余年的基础研究积累,转化为肾祖细胞诱导专利。这不是渐进式改进,而是从0到1的突破,让公司在技术源头建立起壁垒。
第二,分阶段推进。没有一上来就挑战“造器官”的终极难题,而是先以旁分泌机制切入,验证技术、积累数据,再逐步向前推进。
第三,长短结合布局。用小分子(RN-014)对冲细胞疗法(RN-032)的高风险,同时用类器官平台创造技术服务收入,形成稳健的组合。
第四,产学研协同。从京都大学实验室到独立公司,再到与三井化学、阿斯利康等产业巨头合作,每一步都有清晰的资源整合。管理团队由科研背景的長船教授与产业经验的CEO森中顕文共同领导。
第五,资本与政策加持。2024年完成B轮22.5亿日元融资,累计44亿日元,投资方包括三井化学、旭化成等产业巨头。同时入选日本政府J-Startup计划,享有政策倾斜。
5
对中国行业的启示
Rege Nephro的进展,为国内肾脏再生医学领域提供了几点参考:
技术层面,肾祖细胞(NPC)方向值得高度关注。作为诺奖级iPS技术在肾脏再生领域最明确的转化路径,国内外多家企业已在此布局。
策略层面,分阶段转化比一步到位更务实。先解决迫切需求,再攻克终极难题,是控制风险的有效方式。
商业层面,现金流思维不可或缺。用小分子或技术服务对冲细胞疗法的高风险,形成稳健的商业模式,才能支撑长周期的研发投入。
生态层面,产学研协同需要机制保障。从实验室到公司,从合作到融资,每一步都需要清晰的资源整合逻辑。
从技术突破到临床进展,Rege Nephro正在用实打实的步伐,探索诺奖级iPS技术在肾脏再生领域的转化路径。而它所聚焦的核心——肾祖细胞(NPC),正在成为全球肾脏再生医学最受关注的方向之一。
这条赛道,全球高手都在同场竞技。技术路线逐渐清晰,临床验证正在推进。
肾脏再生,正在进入临床倒计时。
参考资料:
1. GBD 2023 Causes of Death Collaborators. Global burden of 292 causes of death in 204 countries and territories and 660 subnational locations, 1990-2023: a systematic analysis for the Global Burden of Disease Study 2023. Lancet. 2025 Oct 18;406(10513):1811-1872. doi: 10.1016/S0140-6736(25)01917-8. Epub 2025 Oct 12.
2. https://mp.weixin.qq.com/s/gBJNhRvcilCSo_9Xicp0QQ
3. https://www.regenephro.co.jp/en/product/
4.https://www.biospace.com/press-releases/rege-nephro-acquires-tamibarotene-related-assets-from-syros-pharmaceuticals-for-u-s-clinical-trials
5. Araoka T, Toyohara K, Ryosaka M, Inui C, Matsuura M, Ma C, Watahiki J, Li Z, Iwasaki M, Watanabe A, Yokokawa R, Tabata Y, Izpisua Belmonte JC, Osafune K. Human iPSC-derived nephron progenitor cells treat acute kidney injury and chronic kidney disease in mouse models. Sci Transl Med. 2025 Apr 2;17(792):eadt5553.