终末期肾病(ESRD)的治疗目前主要依赖透析和肾移植。透析无法完全恢复肾脏复杂的内分泌与代谢功能,且长期透析伴随心血管并发症和生活质量下降;肾移植则面临并发症多、供体短缺等突出问题。再生医学在肾脏领域的应用,通过干细胞、组织工程与生物制造等生物工程技术,构建功能性肾组织以修复或替代受损的肾脏结构,为ESRD的治疗提供了新的可能。
2025年,《Frontiers in Endocrinology》发表了一项范围综述(Scoping Review),系统评估了2004–2024年间再生医学治疗ESRD的临床前研究进展,涵盖111项研究。本文基于该综述,聚焦于肾脏类器官、器官芯片、3D生物打印、异种移植等再生技术,梳理各项技术的证据现状、优势与挑战,以期为关注肾脏再生医学领域的研究者提供参考。
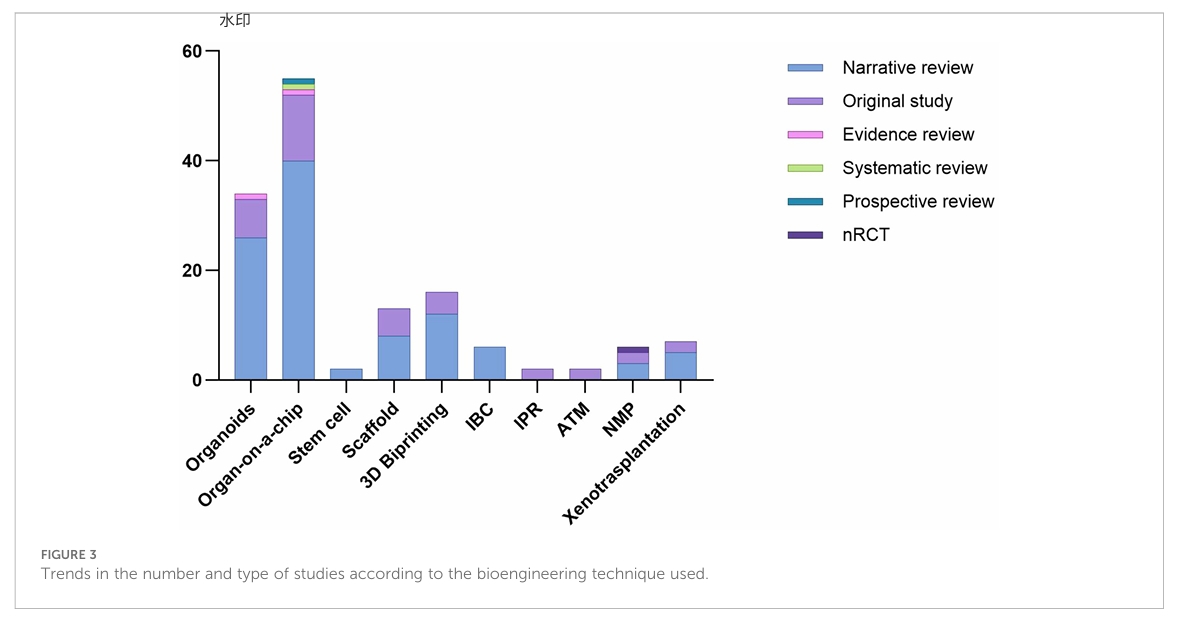
图1. 各生物工程技术的研究数量与类型趋势(点击图片可查看大图)
一、各类再生技术及其研究现状
肾脏类器官(Organoids)是目前研究最为深入的技术方向之一,共纳入34项研究。该类器官利用多能干细胞(如iPSCs)在三维培养条件下自组织形成,可模拟肾单位的多种细胞类型和部分功能,主要用于疾病建模、药物筛选和发育研究。然而,其面临结构复杂、批次间变异大、功能不成熟、缺乏血管网络及成本高等挑战,目前尚难以直接用于临床移植。
器官芯片(Organ-on-a-Chip)是本次综述中研究数量最多的技术,共纳入58项研究。该技术通过微流控系统模拟肾单位的流体剪切力和血流环境,更接近真实生理状态,可用于药物开发、疾病研究和个性化医疗。其主要瓶颈在于生产工艺缺乏标准化、无统一操作协议以及成本较高。
3D生物打印(3D Bioprinting)纳入16项研究。该技术通过逐层沉积细胞、生物材料和生长因子构建三维肾组织结构,可构建微流控设备并生成多种组织类型。当前面临生物墨水选择困难、细胞间距控制不易、成本高及操作人员培训周期长等问题。目前3D生物打印更多用于药物筛选和小型组织构建,距离临床应用尚有距离。
支架技术(Scaffold)共纳入13项研究。该技术利用脱细胞动物肾脏的细胞外基质作为支架,再植入干细胞,具有生物相容性好、可降解可吸收等优势。但面临血栓风险、初始细胞数量要求高、培养系统稳定性差及氧与营养供应困难等挑战。全器官移植体目前仅能在体内支持功能数小时,中远期功能仍需验证。
异种移植(Xenotransplantation)共纳入7项研究。该技术将基因修饰的动物(主要是猪)肾脏移植到人体,有望定制化器官并缩短等待时间。通过多重基因编辑,部分猪肾在非人灵长类模型中已存活超过400天,2023年美国完成了首例活体猪肾移植。然而,该技术仍面临伦理争议、超急性排斥以及人-动物嵌合体带来的未知风险。
常温机械灌注(NMP)共纳入6项研究。该技术在体外用温暖、含氧的血液代用品持续灌注供体肾脏,维持其接近生理状态,可实时评估肾功能并在灌注过程中输送细胞治疗。然而,目前该技术尚未显示出优于传统冷储存的明确证据,且成本较高、操作复杂,更多作为研究工具而非标准临床方案。
囊胚互补(IBC)共纳入6项研究。该技术将供体细胞注入经基因改造而缺乏特定器官的动物囊胚中,利用宿主胚胎的发育环境生成源自供体细胞的人源化器官,有望实现无需免疫抑制的器官定制。然而,该技术面临伦理争议、超急性排斥以及嵌合细胞在宿主体内分布比例难以控制等问题。
祖细胞替代(IPR)共纳入2项研究。该技术不同于囊胚互补,是在肾脏形成阶段而非囊胚期注入供体细胞,可避免注入细胞迁移分布到非靶器官。通过该技术,研究者已在小鼠中同时替代了肾脏的多种细胞谱系。然而,该技术同样面临伦理争议、超急性排斥以及人-动物嵌合体带来的未知风险。
干细胞(Stem Cells)共纳入2项研究。干细胞是具有自我更新和分化能力的未分化细胞,可作为分化细胞的持续来源,对组织形成、维持和修复至关重要。在肾脏再生领域,间充质干细胞是研究最多的类型,主要通过旁分泌机制发挥抗炎、抗纤维化和促血管生成作用。然而,其临床应用的机制尚未完全阐明,需要更多研究明确其旁分泌效应的分子基础。
人工线粒体移植(ATM)共纳入2项实验研究。该技术旨在通过将健康的线粒体注入缺血再灌注损伤的组织,替代受损的线粒体,从而恢复细胞能量代谢。初步研究表明,线粒体移植可能支持肾功能恢复,具有微创治疗的潜力。但该技术证据有限,临床前研究数量少,且大规模可重复生产尚存困难。
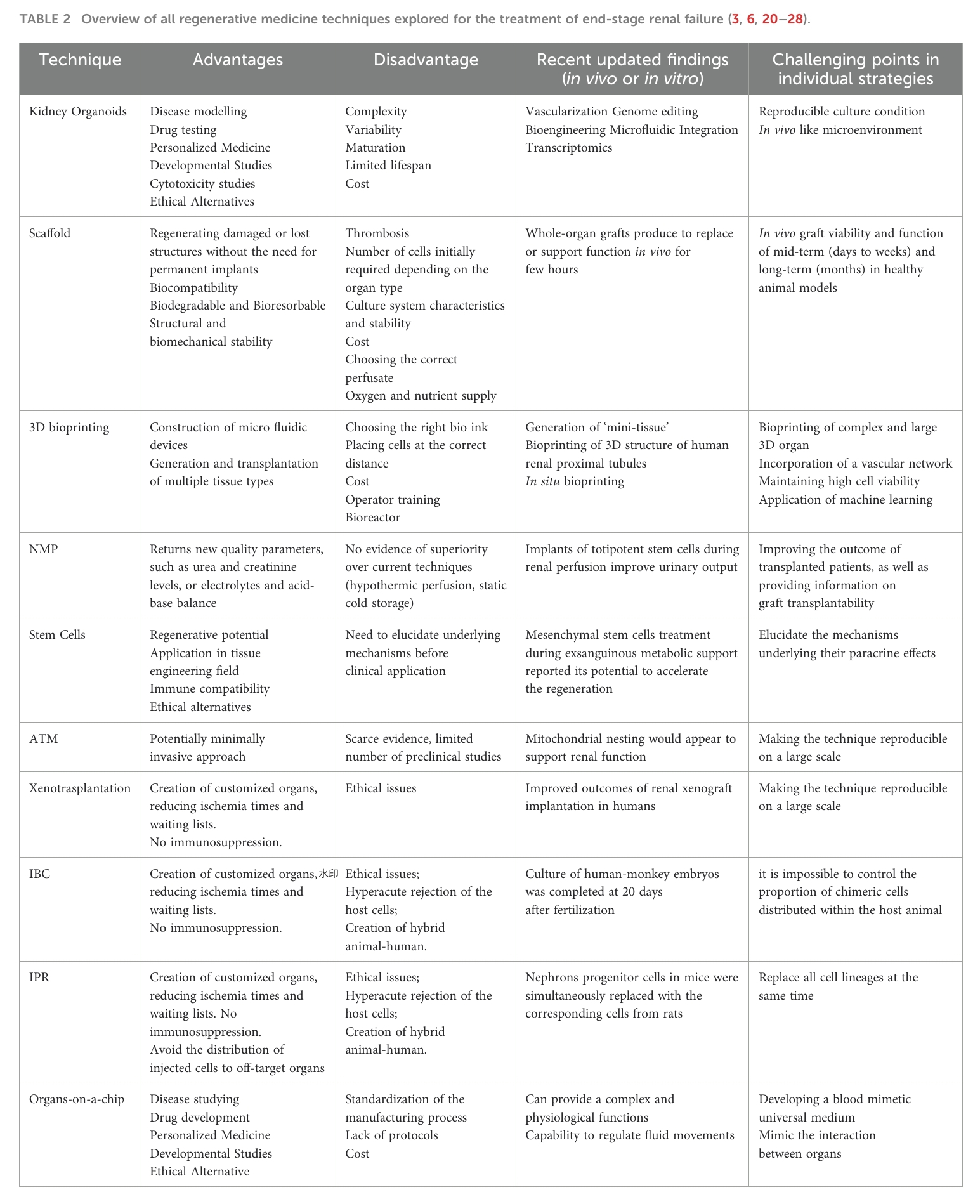
图2. 用于治疗终末期肾衰竭的所有再生医学技术概述(点击图片可查看大图)
二、再生医学在ESRD治疗中的前沿进展与证据基础
肾脏类器官和器官芯片是目前最前沿的两项技术,可模拟肾单位结构和肾脏生理功能,为疾病建模、药物筛选和生物工程肾脏开发提供了平台。该领域的一个里程碑是肾小球芯片的开发,利用iPSC来源的足细胞成功模拟了肾小球滤过和损伤反应。
相比之下,3D生物打印、异种移植、常温机械灌注等其他再生策略仍处于较早期验证阶段。在临床进展较快的策略中,常温机械灌注(NMP)已显示出改善器官保存的效果,但成本极高且未优于传统方法;异种移植方面,猪-灵长类移植通过基因修饰取得了进展,部分模型中移植物存活超过400天,但仍面临蛋白尿、免疫排斥及伦理监管等挑战。
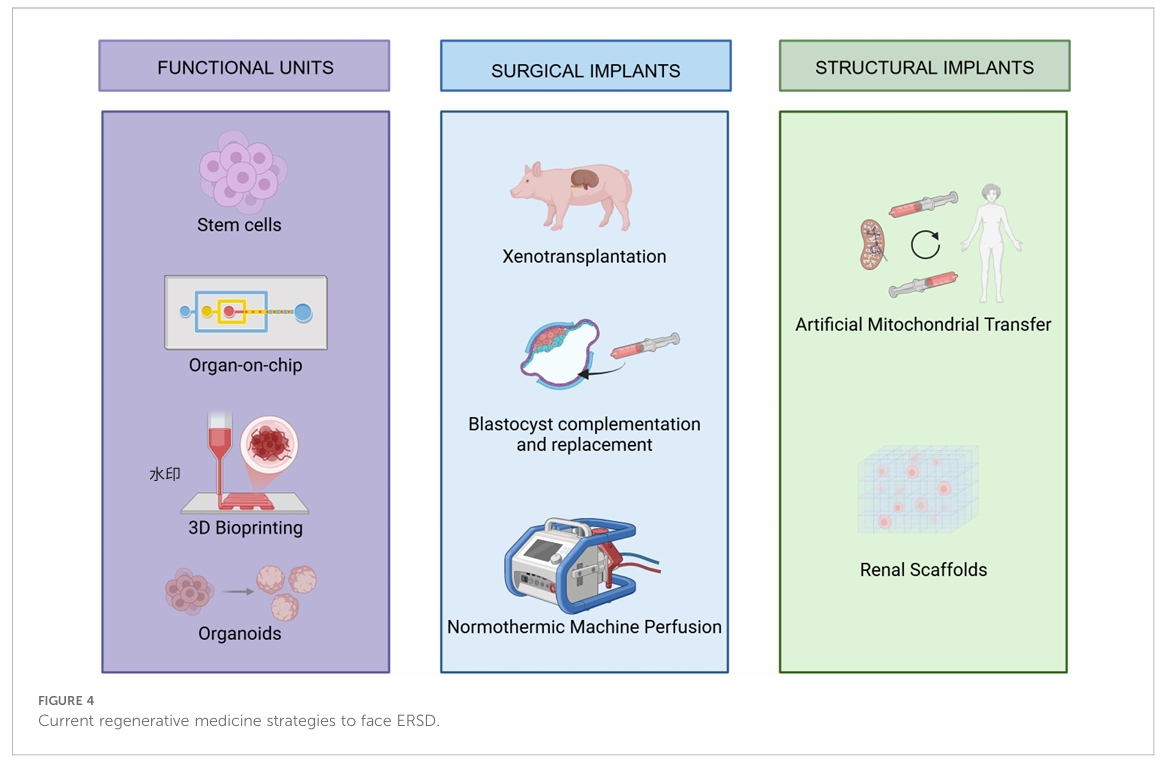
图3. 当前应对终末期肾病(ESRD)的再生医学策略(点击图片可查看大图)
三、共性挑战与未来研究方向
当前文献中叙述性综述居多,缺乏扎实的实验和临床研究,这是制约整个领域发展的核心问题。未来ESRD再生医学的发展受几个关键因素影响:伦理争议、技术能否规模化生产、设备成本和运输储存等实际问题,以及长期安全性和有效性的验证。为此,未来研究应优先开展评估肾脏类器官和器官芯片临床潜力的实验性试验,进行体内研究评估3D生物打印肾组织的功能和整合,并进一步完善异种移植及NMP方案的标准化。
总体而言,肾脏类器官和器官芯片是当前研究最为深入的两项技术,已在药物筛选和疾病建模中展现出实际价值;3D生物打印、异种移植和常温机械灌注等技术虽已进入人体测试阶段,但仍需进一步验证和标准化。该综述的价值在于,它不仅系统勾勒了各项技术的证据现状与转化障碍,更明确指出当前研究以叙述性综述为主、缺乏高质量实验研究的核心短板。未来,实证验证、跨学科合作与伦理监管的协同推进,将是这些创新从实验室走向临床的关键所在。
参考文献:
Vigezzi A, Brani P, Dalla Gasperina D, Azzi L, Giaroni C, Inversini D, Pettinato G, Massaad M, Carcano G, Ietto G and Baj A (2025) Preclinical approaches in regenerative medicine for treating end-stage renal disease: a scoping review. Front. Endocrinol. 16:1549744



