近日,陆军军医大学曾文教授团队,联合华中科技大学同济医学院、重庆大学等研究机构,在生物材料领域权威期刊《Biomaterials》(IF 12.9)上发表创新研究,成功开发出一种名为“Needlepatch(针贴片)”的工程化肾复合贴片,通过程序化治疗策略,显著改善了急性肾损伤的预后。
急性肾损伤(AKI)是临床上常见的危重病症,其特点是肾功能急剧下降,导致全身并发症,发病率和死亡率显著升高。据统计,41.2%的AKI患者在出院时仍存在肾功能损害,这一群体的1年死亡率高达60%。AKI的病理特征之一是持续性炎症微环境,这导致微血管稀疏和纤维化,推动肾损伤向慢性肾病和终末期肾病进展。
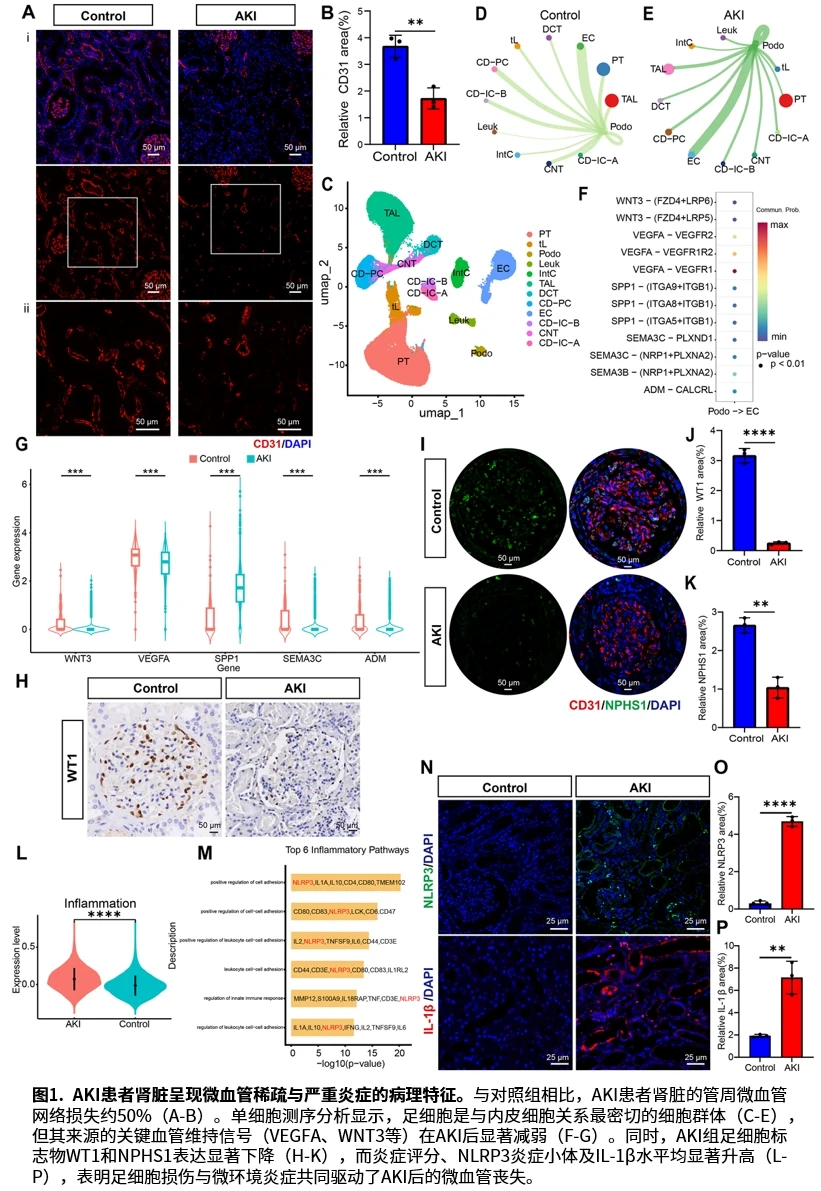
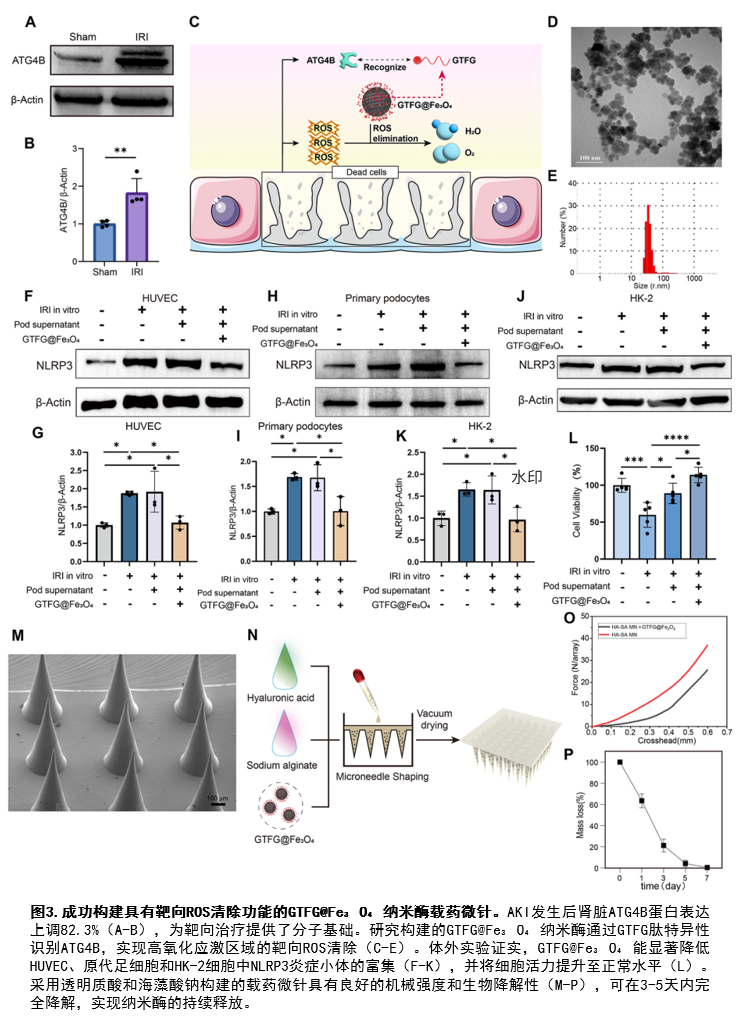
研究团队通过分析人类AKI样本发现,AKI发生后肾脏的管周微血管网络损失约50%。单细胞RNA测序数据分析揭示,足细胞是与内皮细胞关系最密切的细胞群体,其来源的血管维持信号在AKI后普遍减弱。同时,AKI发生后ATG4B蛋白表达上调82.3%,NLRP3炎症小体和IL-1β表达上调超过3倍。
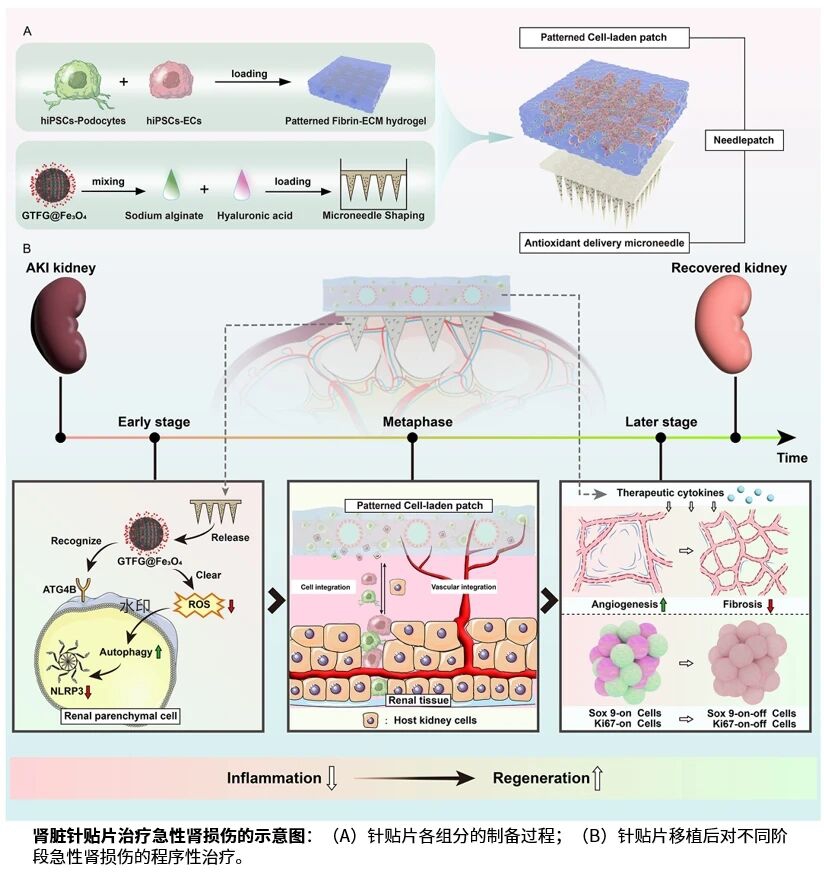
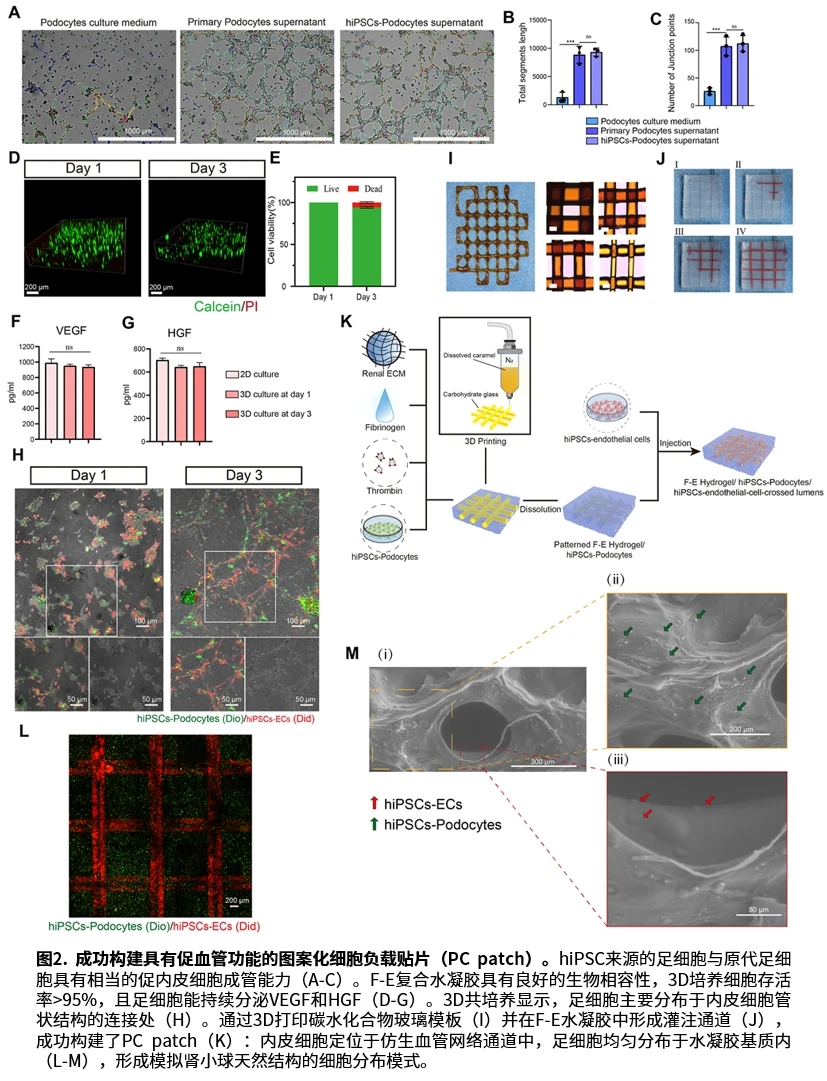
针对这一病理特征,研究团队构建了由两个模块组成的Needlepatch:装载GTFG@Fe₃O₄靶向纳米酶的抗氧化递送微针,以及通过3D打印技术构建的图案化细胞负载贴片。前者通过GTFG肽特异性识别ATG4B蛋白,在高氧化应激区域精准清除活性氧;后者将hiPSC来源的内皮细胞和足细胞分别定位于仿生血管网络和管状结构连接处,模拟肾小球天然结构。
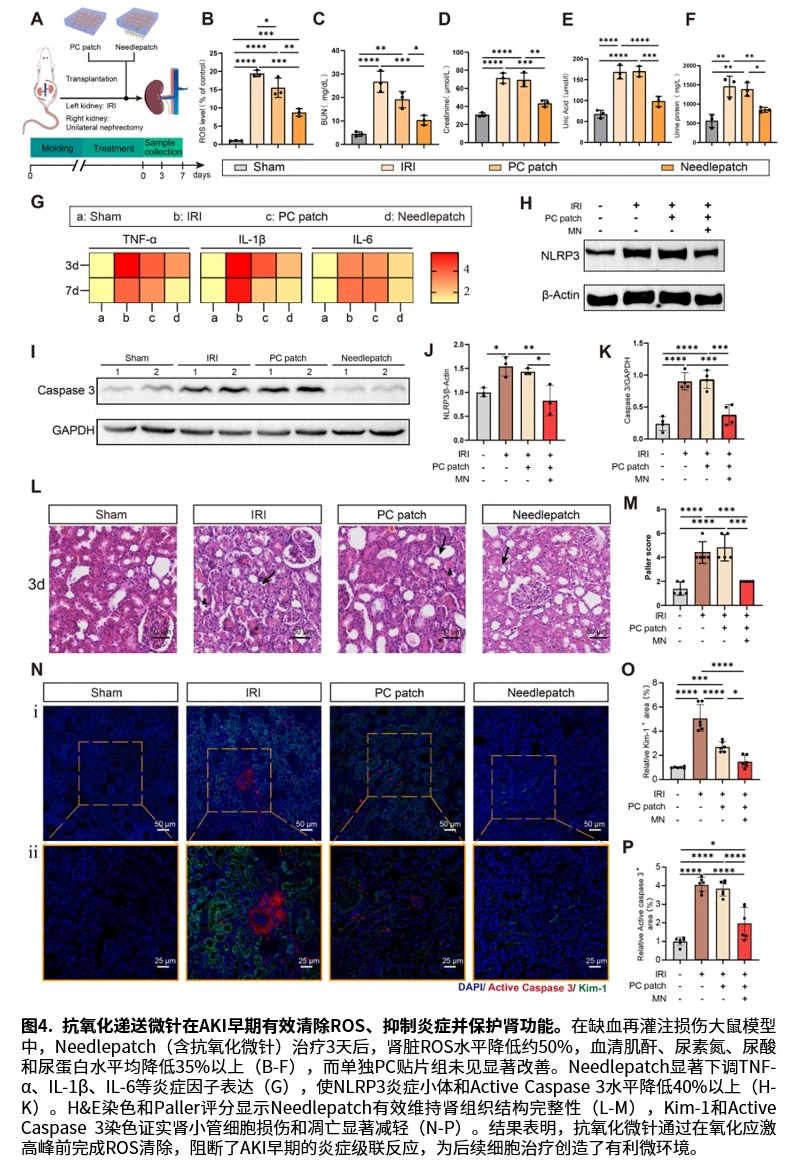
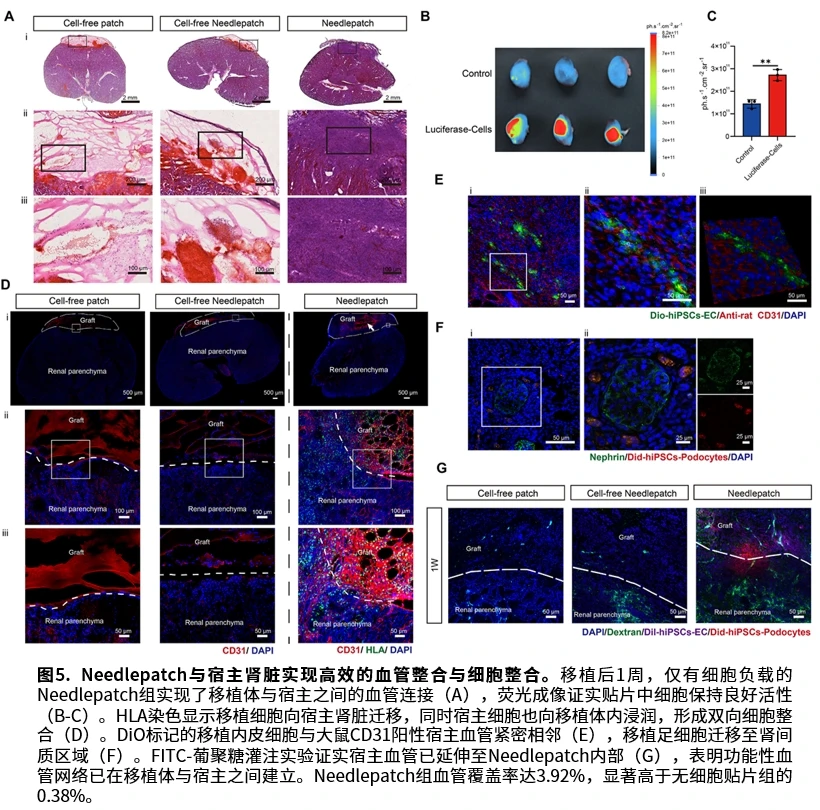
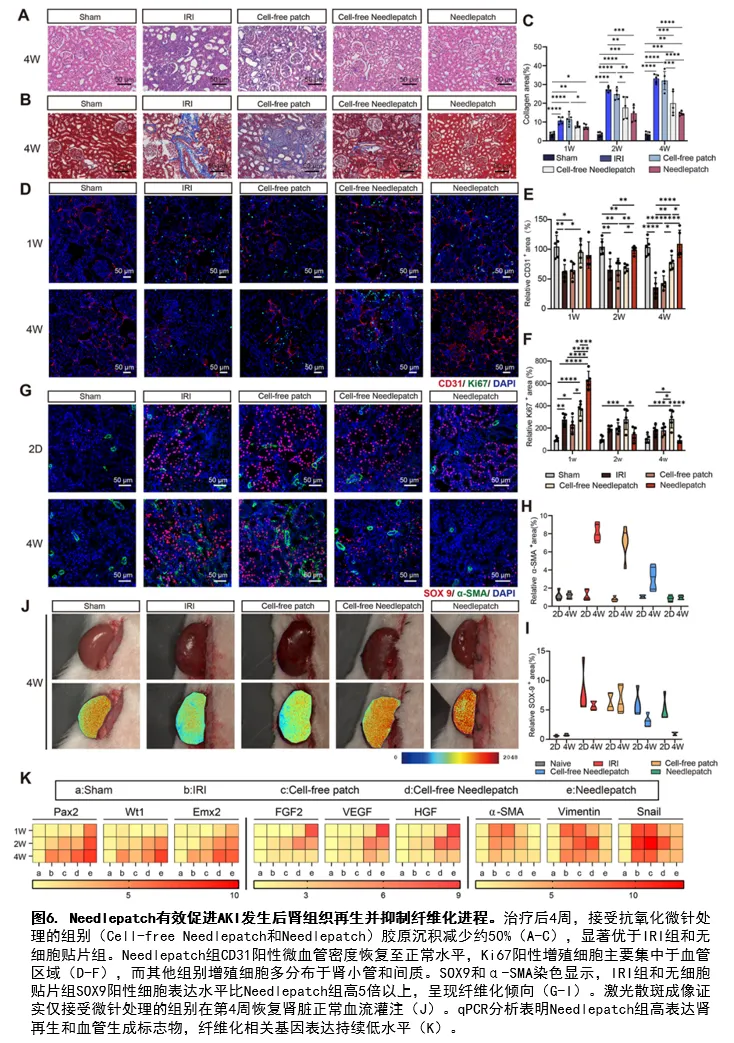
在缺血再灌注损伤大鼠模型中,Needlepatch表现出显著疗效。治疗后第3天,肾脏活性氧水平降低约50%,血清肌酐、尿素氮、尿酸和尿蛋白水平均降低35%以上,NLRP3和IL-1β表达降低40%以上。治疗后第4周,抗氧化递送微针处理组别中的胶原沉积减少50%,Needlepatch组的血管覆盖率达3.92%(无细胞贴片组仅0.38%),SOX9阳性细胞表达水平降低5倍以上。
该研究通过程序化、多维协调的干预策略,实现对AKI的精准治疗,为急性肾损伤及其他复杂实质器官疾病的治疗提供了新的转化思路。

参考文献:
Zhao X, Li X, He L, Gong X, Wang Y, Chen L, Tian H, Wang Y, Xu X, Sheng T, Liu M, Li J, Liu D, Li L, Zhao W, Zeng W. Engineered Needlepatch for the treatment of acute kidney injury. Biomaterials. 2026 Jun;329:123936. doi: 10.1016/j.biomaterials.2025.123936.