摘要:终末期肾病(ESRD)的治疗长期受限于透析与移植的不足,而干细胞与生物工程技术的兴起为肾脏再生带来了全新可能。近日,一篇发表于Stem Cell Research的系统综述全面评估了该领域的进展与挑战。本文基于该综述内容,梳理干细胞疗法的多类来源与作用机制,解读生物工程技术在肾脏结构构建中的关键应用,并系统分析其在临床转化中的科学路径与现存障碍。

终末期肾病(ESRD)是全球性的重大健康负担,目前依赖透析和肾移植的治疗方式存在诸多限制。透析无法完全恢复肾脏复杂的内分泌与代谢功能,且长期透析伴随心血管并发症和生活质量下降。肾移植虽能改善预后,但受限于供体短缺、手术相关并发症及长期免疫抑制治疗的风险。因此,以干细胞为基础的再生医学被认为是具有潜力的下一代治疗策略。
近期发表于Stem Cell Research的综述《Stem Cell and Bioengineering Approaches for End-Stage Renal Disease: A Comprehensive Review》系统梳理了该领域当前的科学证据、技术路径与现存挑战。该综述基于现有临床前研究及早期临床试验数据,客观评估了干细胞疗法与生物工程技术在ESRD治疗中的潜在应用价值与转化障碍。
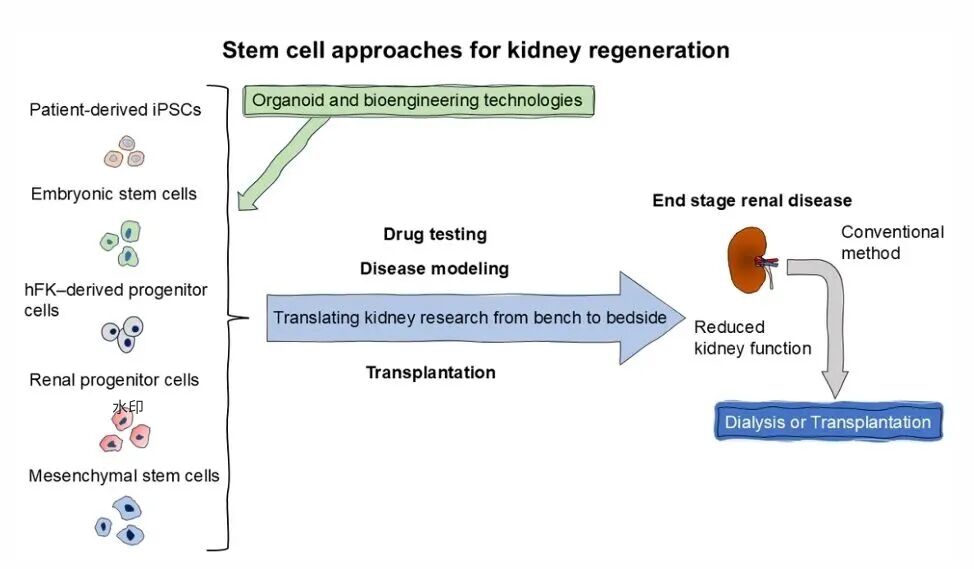
图形摘要
干细胞来源与各自潜力
目前研究主要聚焦于四类干细胞:
胚胎干细胞(ESCs):具有多向分化潜能,可通过模拟发育信号(Wnt, BMP, FGF)分化为肾脏前体细胞并形成三维肾脏类器官。这些类器官是研究发育、疾病机制和药物测试的有价值工具。但ESCs存在伦理争议、致瘤风险及免疫排斥问题,且生成的类器官在血管化和功能成熟方面尚不完善,目前主要用于基础研究。
诱导多能干细胞(iPSCs):由体细胞重编程获得,避免了伦理问题,并可能实现自体移植减少排斥。iPSCs可被诱导形成肾脏类器官,用于遗传性疾病(如多囊肾病、Alport综合征)建模和药物肾毒性评估。其临床应用同样面临类器官功能不成熟、血管化不足、致瘤风险及标准化生产等挑战。
间充质干细胞(MSCs):从骨髓、脂肪等多组织获取,主要通过旁分泌机制(抗炎、抗纤维化、促血管生成)发挥肾脏保护作用。临床前模型显示其在急性肾损伤和糖尿病肾病中具有改善作用。早期临床试验报告了良好的安全性,并观察到初步的疗效信号,但仍需优化给药方式、剂量和验证长期效果。
肾脏前体细胞(RPCs):指存在于肾脏内(如鲍曼氏囊附近)或可从尿液中分离的、具有干细胞样特性的细胞群。它们具有向肾实质细胞分化的倾向,被认为是具有潜力的自体细胞来源,但其增殖分化能力的稳定性及长期修复效力仍需在体内验证。
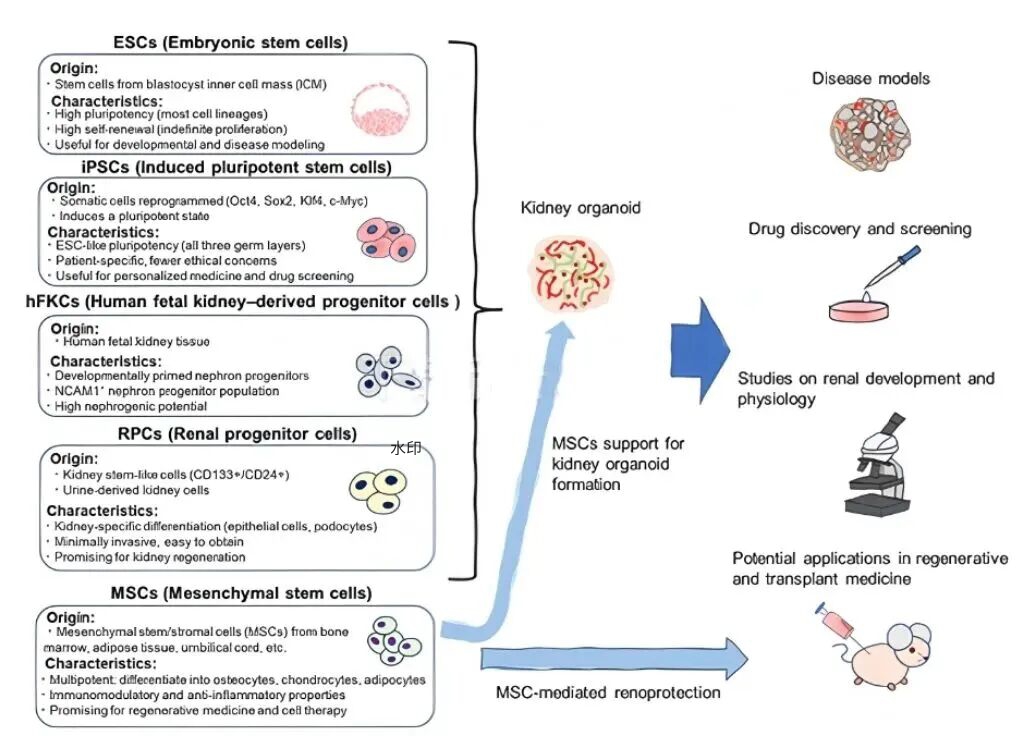
图2. 从多种干细胞来源(包括胚胎干细胞、诱导多能干细胞及成体干细胞)产生肾脏类器官的诱导流程及其多维度应用场景,涵盖了从疾病建模、药物筛选到再生治疗的全链条研究路径。
生物工程技术:构建结构与功能
肾脏复杂的结构使得其再生极具挑战。生物工程技术旨在构建或支持功能性肾脏组织。
肾脏类器官:通过引导多能干细胞在三维条件下自组织形成。当前主要瓶颈在于血管化不足和功能不成熟。移植至体内促进血管生成、与内皮细胞共培养以及优化培养条件是主要的解决策略。
工程化构建:
3D生物打印:用于精确排列细胞,构建肾小管和血管网络等结构。
脱细胞支架:使用脱细胞动物肾脏的细胞外基质作为支架,重新植入干细胞,以生成可移植的生物人工肾。
肾脏芯片:利用微流控技术模拟肾脏的流体环境,用于药物肾毒性测试和细胞反应分析
作用机制:旁分泌与直接再生
干细胞疗法的作用机制主要分为两类:
旁分泌机制:干细胞分泌生物活性因子(如抗炎因子、生长因子),调节肾脏微环境,促进内源性保护和修复。这在早期或中度肾损伤中起主要作用。
直接再生机制:干细胞直接分化为肾脏细胞并整合,以替代受损组织。这在肾单位大量丢失的ESRD中被认为是必需的。目前共识认为,旁分泌效应是许多干细胞疗法(尤其是MSCs)的主要作用方式。
临床前与临床研究现状
临床前证据:大量动物研究表明,特别是MSCs,能改善急性肾损伤和慢性肾病模型中的肾功能、减轻损伤。但多数研究并非针对真正的ESRD模型,在终末期肾衰竭中直接有效的证据有限。
临床试验:MSCs疗法的早期临床试验(主要针对慢性肾病和糖尿病肾病)显示了可接受的安全性,部分报告了肾功能或蛋白尿的轻微/短暂改善。迄今为止,尚无专门针对长期透析ESRD患者的临床试验,在该人群中有效的证据缺乏。
iPSC/类器官方法:目前主要用于疾病建模和药物筛选。临床前移植研究显示了潜力,但将其直接外推至ESRD面临挑战,且血管化、成熟度、免疫兼容性、致瘤风险和规模化生产等关键转化障碍尚未解决。
主要挑战与未来方向
综述指出,临床转化面临五大关键挑战:
血管网络构建:体外无法实现功能成熟的肾血管网络。
安全性与免疫:iPSC存在致瘤风险;自体iPSC生产存在时间、成本和基因组稳定性问题。
标准化生产:需要建立符合GMP标准的可重复、规模化生产工艺。
针对ESRD的证据:缺乏干细胞或类器官对ESRD有效的直接临床前或临床证据。
功能成熟:使类器官获得成人肾脏样功能。
未来,成人肾脏来源细胞组装的三维球体被认为是一种有前景的替代策略,可能主要通过旁分泌信号发挥作用,在安全性、免疫兼容性和转化可行性上具备优势。研究重点应包括确定关键生物活性因子、优化基于球体的方法、标准化治疗方案,以及开展精心设计的大规模随机对照试验。
干细胞与生物工程方法为终末期肾病治疗带来了新的希望。MSCs疗法在安全性上已取得初步验证,iPSC与类器官技术在疾病建模和药物开发中展现出强大潜力。然而,从实验室到临床,特别是针对ESRD的治疗,仍有一段长路要走。克服血管化、功能成熟、安全性和规模化生产等核心挑战,并通过严谨的临床试验验证疗效,是将这些前景转化为现实临床应用的关键。
参考文献:
Nishimura Y. Stem Cell and Bioengineering Approaches for End-Stage Renal Disease: A Comprehensive Review. Stem Cells. 2026 Jan 12:sxag003.