01.导语
肾脏疾病正成为全球性的健康挑战,而传统的透析和移植方案远不能满足日益增长的患者需求。再生医学领域的科学家们正将目光投向一个充满希望的方向:利用干细胞培育出可供移植的功能性肾脏组织。
近期发表于 Nature Biotechnology (IF 41.7)的文章《Developmentally inspired synthetic kidney engineering》(受发育启发的合成肾脏工程),系统性地提出了一种名为 “发育工程” 的全新策略,为再生医学领域指明了关键技术路径。
02.当前瓶颈:类器官的“自组织”潜力与局限
干细胞来源的肾脏类器官是近年来的重大突破,它们能够在一定程度上模拟肾脏的复杂结构,如肾单位和集合管。然而,目前的类器官主要依赖细胞内在的“自组织”能力,这导致了几个核心挑战:
•结果不可控:类器官之间存在显著的变异性。
•细胞类型缺失:缺乏关键的基质细胞和完整的血管系统。
•功能不成熟:无法实现真实肾脏的复杂滤过、重吸收和内分泌功能。
•难以规模化:缺乏构建临床所需组织规模的可靠方法。
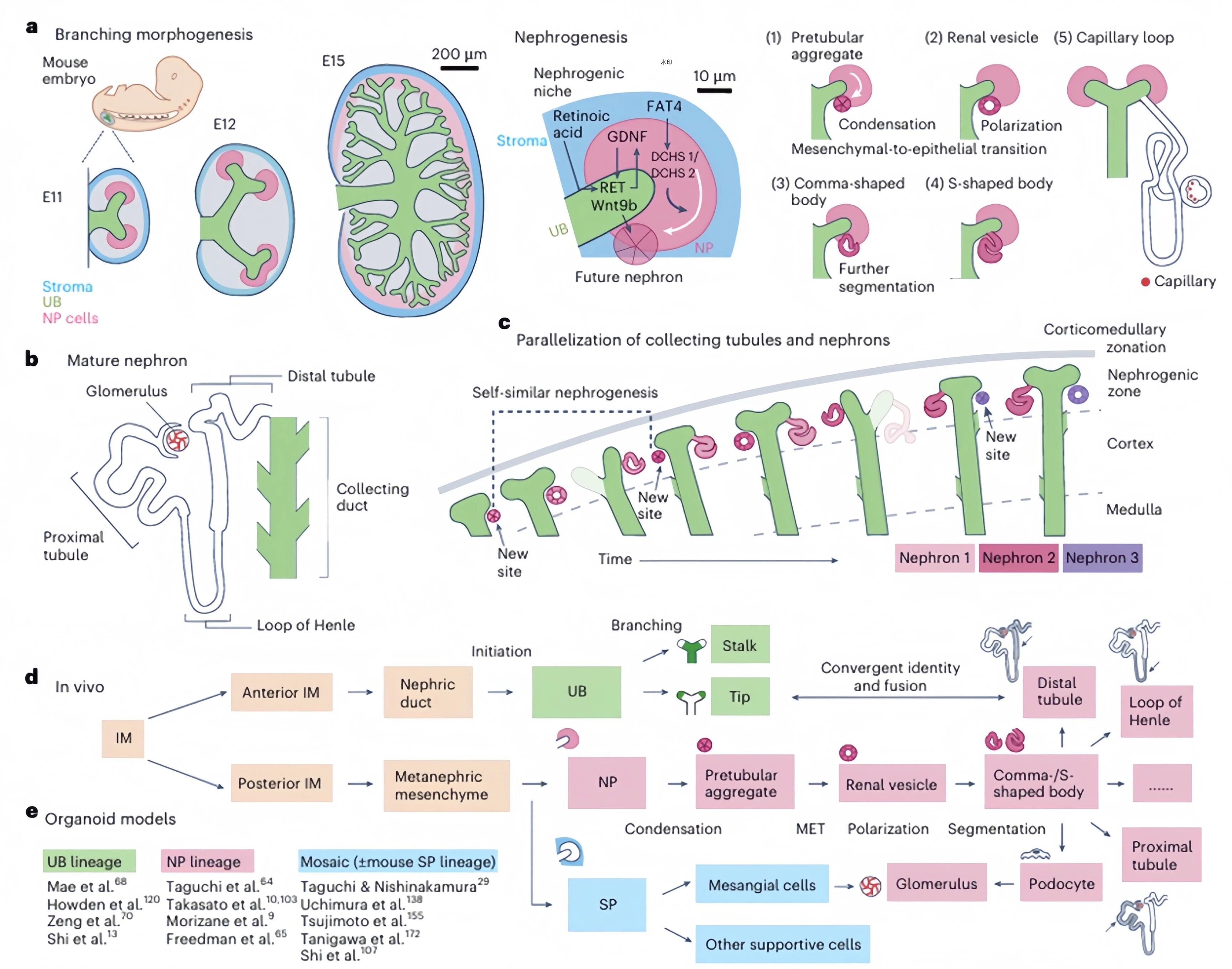
图1. 通过对比体内肾脏发育的并行化结构与体外类器官现状,揭示后者尚未实现通过分支持续创造新龛位、进行多轮肾单位生成的规模化能力。
03.破局之策:“发育工程”理念的提出
解决这些瓶颈的关键在于向“胚胎发育”学习。肾脏在体内发育时,并非单纯地自我组织,而是在一系列精心编排的空间和时间信号引导下,一步步构建起其精密的并行化结构和多样化功能。
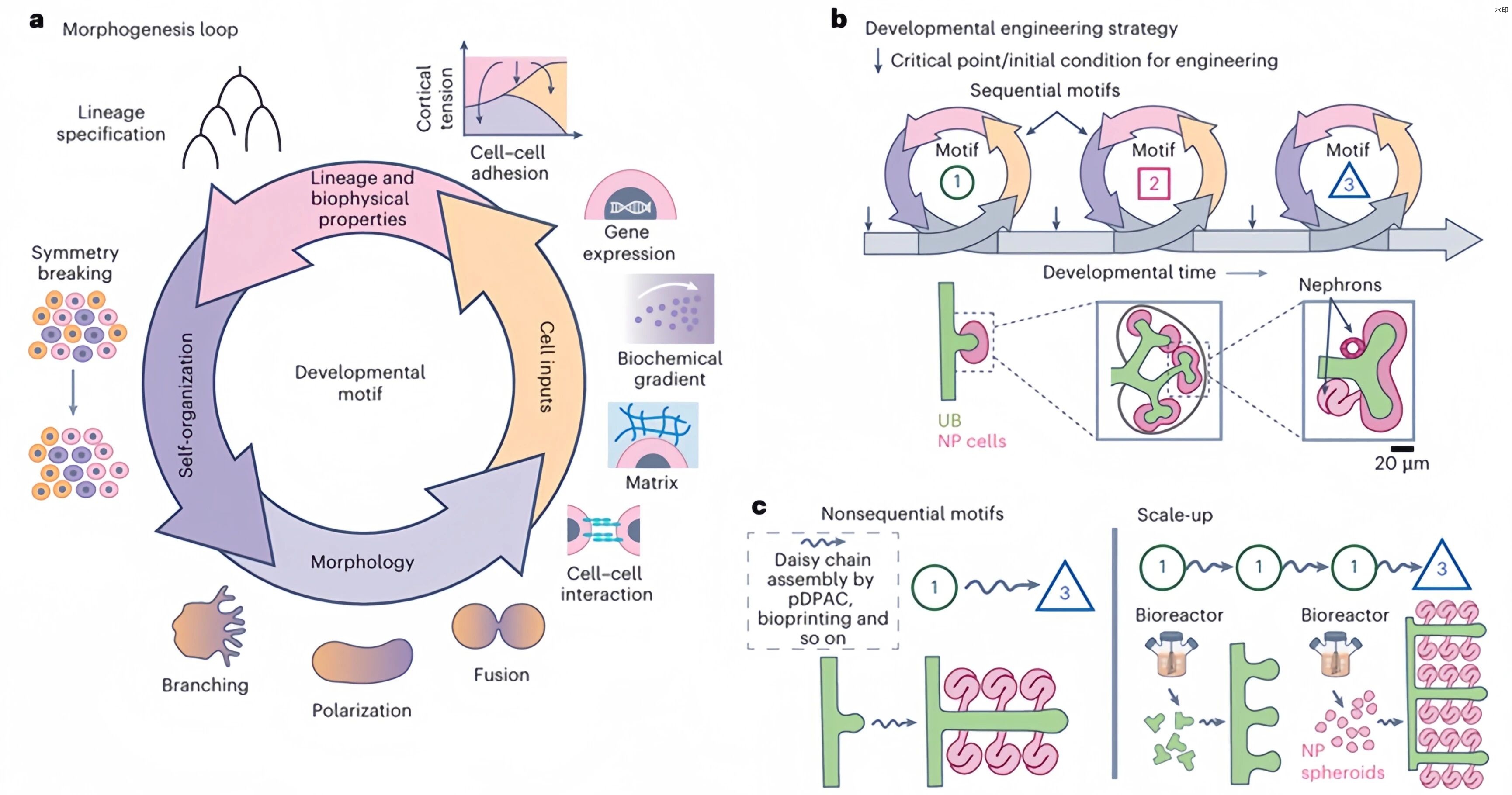
图2. 完整呈现了“发育工程”策略的方法论框架:识别发育关键“基序”,在体外模拟其初始条件,引导自组织形成结构单元,再通过直接组装将不同基序的结构单元“串联”,构建更大尺度、功能集成的人造组织。
“发育工程”策略的核心思想,就是模仿这一过程:通过人为设置精准的“初始和边界条件”,引导干细胞群体完成特定发育阶段(即“基序”)的自组织,然后将这些“基序”模块化地连接起来,最终构建出高度复杂且功能集成的人造肾脏组织。
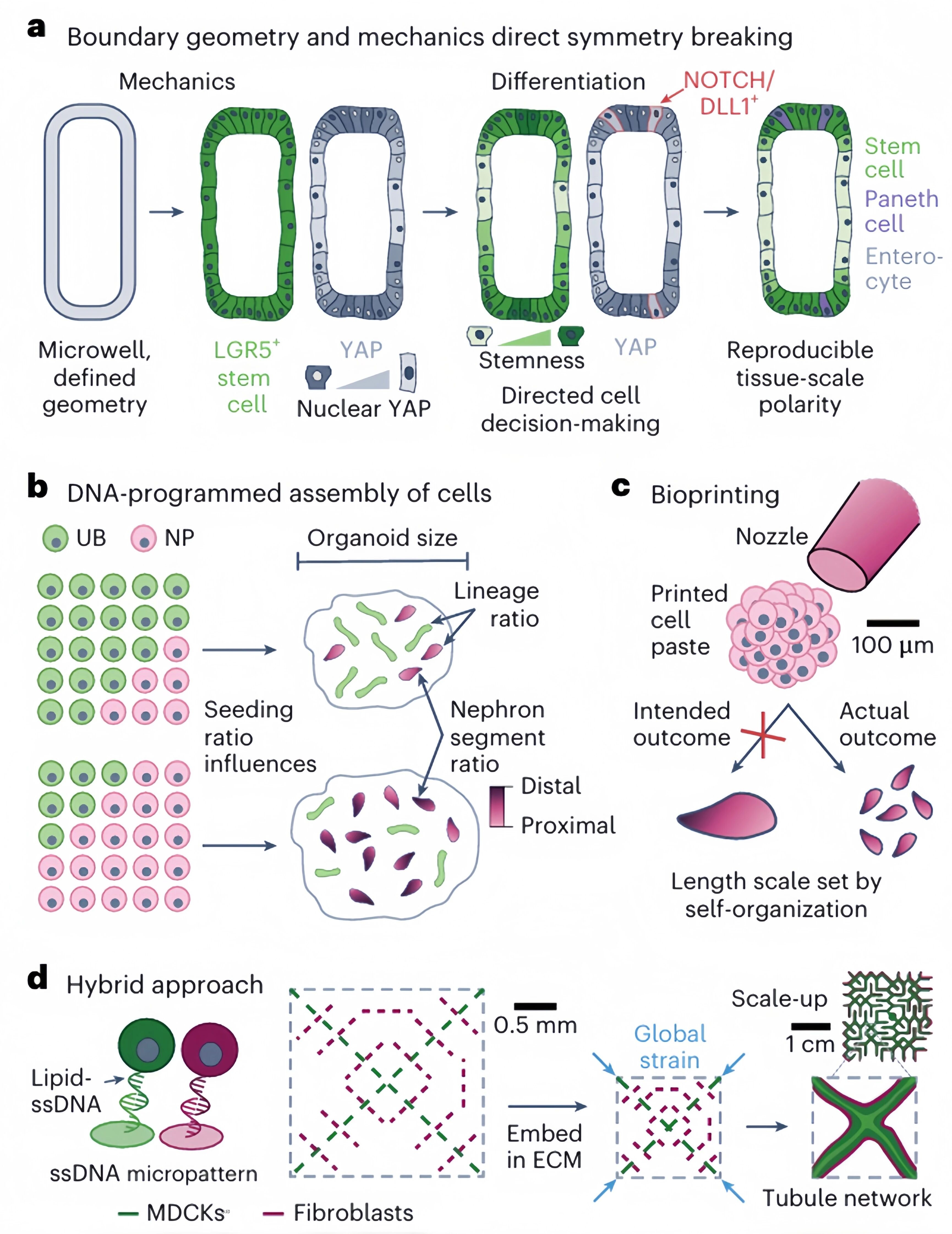
图3. 通过四个示例系统展示了如何通过工程手段设置初始条件(几何边界、细胞组成、打印尺度、机械应变)来引导和控制发育基序的自组织过程,为“发育工程”策略的具体实施提供了技术工具箱和设计思路。
04.关键技术解读:从理念到实践
从临床转化和产业化的角度来看,文中提到的几项关键技术尤为值得关注:
1. 精准设定“初始条件”:从源头掌控组织命运
•细胞编程性组装:研究提到的pDPAC技术,利用DNA链的“魔术贴”效应,能以单细胞精度精准排列不同种类的肾祖细胞。这为模拟发育初期肾单位祖细胞与输尿管芽的精确空间位置关系提供了可能,直接影响后续肾单位的分化类型和比例。
•生物打印的尺度挑战:3D生物打印是构建大块组织的希望,但打印精度(~50-200微米)与单个肾单位的自组织尺度(~50-200微米)存在错配。文章指出,直接将细胞打印成团,会引发多个而非一个肾单位形成。因此,更可行的策略是将生物打印用于更大尺度的结构组装,而微观结构的精细构建则依赖于细胞自身在引导下的自组织。这为工程技术开发提供了重要思路。
2. 智能化引导细胞身份:从被动分化到主动操控
•合成组织者细胞:这是一个极具想象力的工具。通过基因工程改造的“合成组织者”细胞可以分泌特定形态发生素(如WNT),在类器官内部建立局部信号梯度。实验证明,这能成功引导早期肾单位进行定向极化,并调控其近端与远端小管的比例。这为构建具有统一方向、可连接性的平行肾单位阵列铺平了道路。
•光遗传学:利用光来精确控制特定信号通路(如RET(Receptor Tyrosine Kinase,受体酪氨酸激酶)的激活时间和位置。这对于实现肾脏发育中关键的、持续多代的输尿管芽分支形态发生至关重要,有望解决当前类器官只能进行一两次分支的难题。
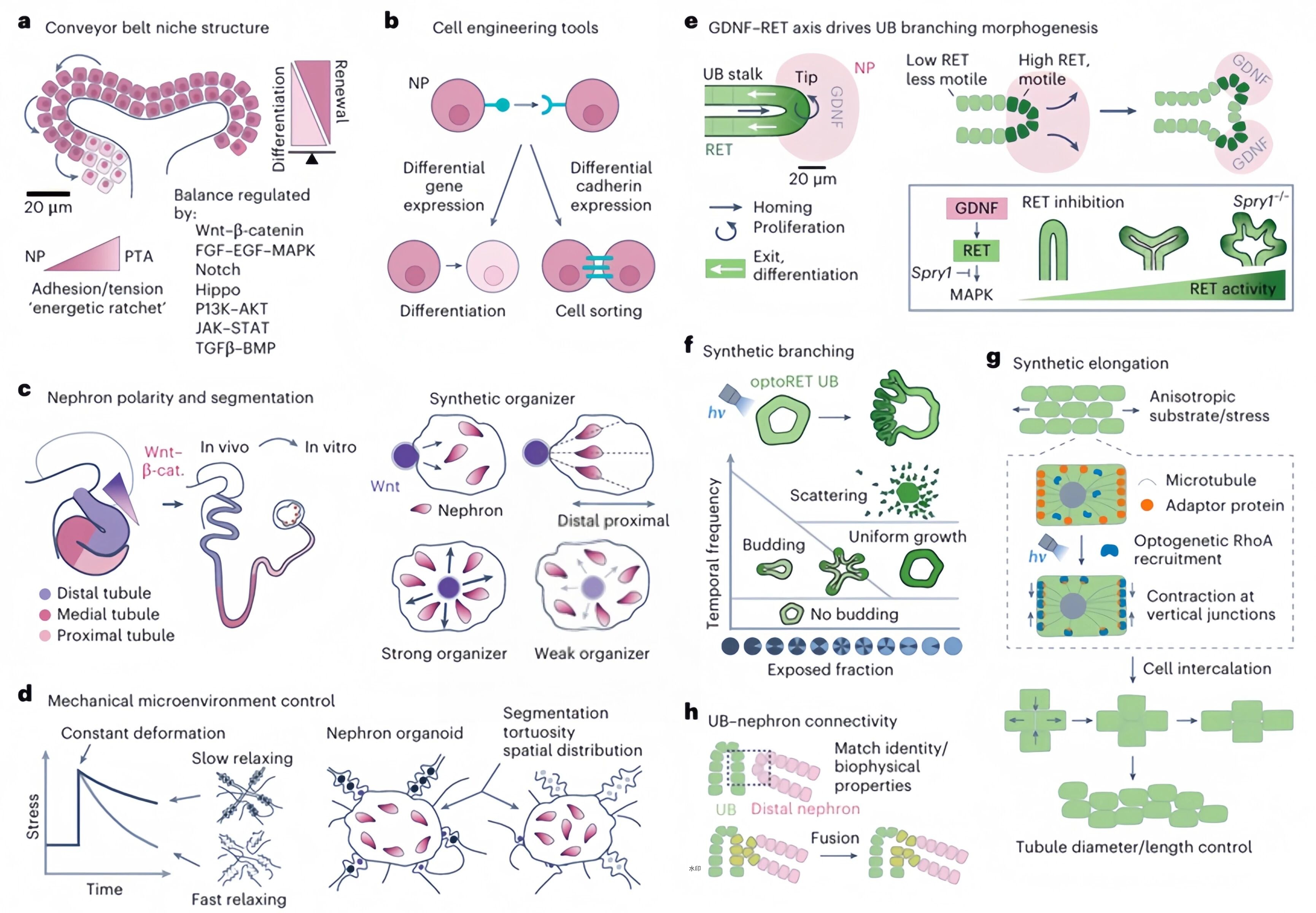
图4. 系统梳理了针对NP(肾单位祖细胞)和UB(输尿管芽)两大谱系的发育工程策略,涵盖信号调控(SynNotch、合成组织者、光遗传学)、物理微环境(基质力学)、细胞行为控制(粘附力、皮层张力)等多个维度,并提出了实现持续性肾单位生成、多代分支形态发生、肾单位-集合管高效融合的具体技术路径。
3. 解决关键生物学难题:构建完整功能单元
• 基质细胞不可或缺:研究强调,长期以来被忽视的基质细胞对维持肾单位祖细胞的自我更新和分化平衡至关重要。目前人类基质细胞系的分化仍是空白,一旦突破,将极大提升类器官的结构层次和功能成熟度。
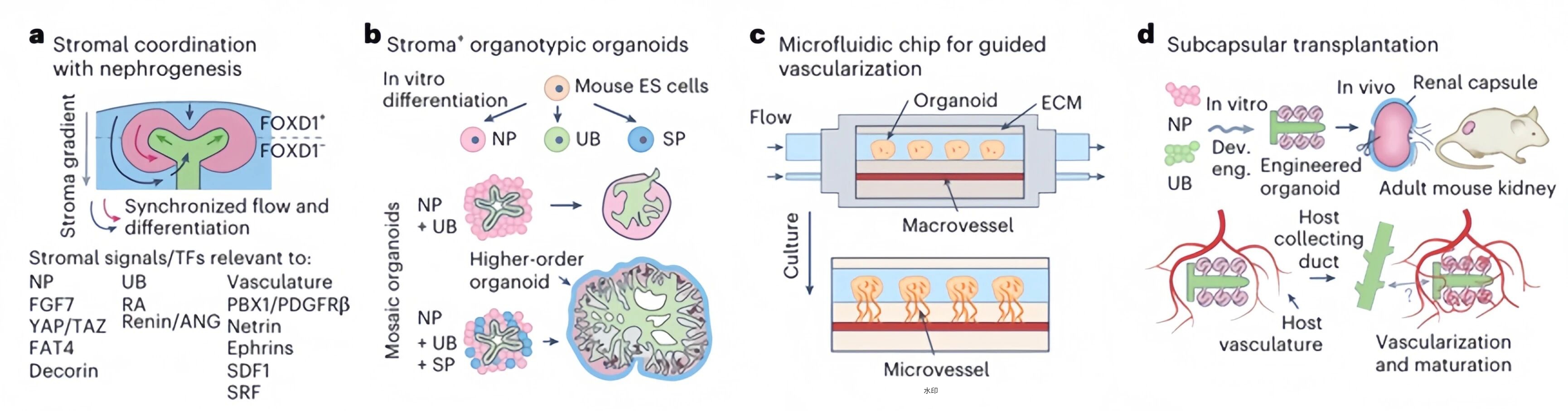
图5. 系统阐述了基质谱系在肾脏发育中的关键调控作用,指出目前人类基质细胞分化的缺失是类器官结构层次提升的主要瓶颈。同时展示了两种血管化路径——体外微流控构建可灌注网络与体内移植后宿主血管侵入——为未来构建功能完整的合成肾脏组织提供了技术方向。
•实现“肾单位-集合管”精准对接:这是构建有功能排泄通路的最后一步。研究表明,通过优化两类祖细胞的空间位置和诱导其身份趋同,可以实现高效的自发融合与管腔连通。这为最终构建一个拥有统一尿液出口的肾脏组织奠定了基础。
05.未来展望:从实验室走向临床
这篇研究为肾脏再生医学的研发方向提供了强有力的理论支持和前沿技术参考。未来的合成肾脏组织不会是简单的细胞堆砌,而是如同精密仪器一般,在各个关键节点被精确引导、组装而成的生命体。
“发育工程”策略提示我们,通过整合精准的细胞编程、创新的生物材料、智能的合成生物学工具和先进的生物打印技术,有望逐步克服当前类器官的局限性,最终构建出能够真正替代肾脏功能、为患者带来高质量生命延续的生物人工器官。
参考文献:
Warrner E, Huang AZ, Hughes AJ. Developmentally inspired synthetic kidney engineering. Nat Biotechnol. 2026 Feb 10. doi: 10.1038/s41587-026-03011-9. Epub ahead of print. PMID: 41667710